题目内容
【题目】根据图1和图2回答下列问题。
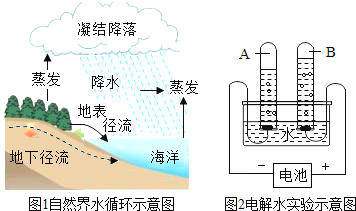
(1)图1的海水中含有大量氯化钠,氯化钠是由(填离子符号)_____和_____构成;
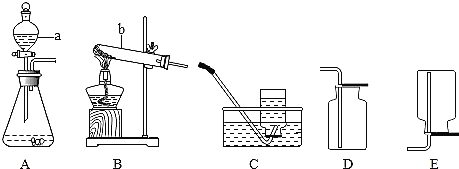
(2)图2的试管A中的气体的化学式是_____,试管B中气体的检验方法是_____;
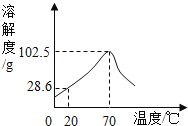
(3)分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母序号,下同)_____;
A.水分子不断运动 B.水分子之间间隔不变 C.氢、氧原子不发生改变 D.水分子可以保持水的物理性质
【答案】Na+;Cl﹣;H2;将带火星的木条伸入该气体中,观察到木条复燃,则该气体是氧气;AC;
【解析】
(1)根据海水中的物质为氯化钠来分析其构成;
(2)根据电解水实验可知A中气体的体积大,则A为氢气,B为氧气,利用氧气的性质来检验;
(3)水蒸发的过程,水分子不变,分子中的原子不变,利用分子的性质来分析解答。
(1)因氯化钠属于盐类化合物,则氯化钠是由钠离子和氯离子构成的,离子符号分别为Na+和Cl-;
(2)因电解水生成氢气与氧气的体积比为2:1,显然A中气体多,则A为氢气、B为氧气,又氧气具有助燃性,能使带火星的木条复燃,则可以将带火星的木条伸入该气体中,观察到木条复燃,则该气体是氧气;
(3)因在水蒸发的过程中,水分子不变,则水分子的体积不变,分子中的原子不变,而水由液体变为气体时水分子之间的间隔变大,且蒸发过程中水分子不断运动,故选AC。

练习册系列答案
相关题目