题目内容
26g黄铜(Cu-Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为125.8克。求:⑴黄铜中铜的质量分数;⑵反应后所得溶液中溶质质量分数。(计算结果精确到0.1%)
解:氢气的质量为0.2克。
设锌的质量为X,
Zn+ H2SO4 = ZnSO4+ H2↑
65 161 2
X Y 0.2g
65:X=2:0.2g X=6.5g
161:Y=2:0.2g Y=16.1g
黄铜中铜的质量分数: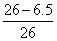 ×100%=75%
×100%=75%
反应后所得溶液中溶质质量分数: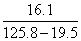 ×100%=15.1%
×100%=15.1%
答:黄铜中铜的质量分数为75% 反应后所得溶液中溶质质量分数为15.1%

练习册系列答案
相关题目