题目内容
【题目】如图所示,A是氧化物,可作干燥剂;D是一种盐,用于制造玻璃,洗涤剂等,它们之间发生如图变化,请你根据所学的化学知识作出推断: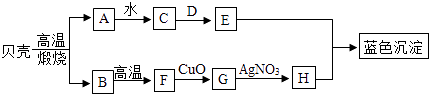
(1)写出化学式:A , D;
(2)贝壳高温煅烧的化学方程式;
(3)B→F的化学方程式;所属的基本反应类型是;
【答案】
(1)CaO;Na2CO3
(2)CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
(3)CO2+C ![]() 2CO;化合反应
2CO;化合反应
【解析】贝壳的主要成分为碳酸钙,高温煅烧生成氧化钙、二氧化碳,A是氧化物,可作干燥剂,则A为CaO,B为CO2;A与水作用生成C即C为Ca(OH)2;D是一种盐,用于制造玻璃,洗涤剂等,D为Na2CO3;E为NaOH;B高温生成F,F为CO;G为Cu;H为Cu(NO3)2根据题意知道贝壳的主要成分是碳酸钙,D为Na2CO3,蓝色沉淀为氢氧化铜。
贝壳(碳酸钙)高温分解为CaO和CO2,A为干燥剂,即为CaO,B为CO2,CaO和水反应生成氢氧化钙,即C为Ca(OH)2,Ca(OH)2和Na2CO3反应生成碳酸钙和NaOH,即E为NaOH。
CO2高温可以和碳反应生成CO,即F为CO,CO和氧化铜反应生成Cu和CO2,即G为Cu,Cu和硝酸银反应生成银和Cu(NO3)2,即H为Cu(NO3)2

 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案【题目】为了测定黄铜(铜、锌合金)中铜的质量分数,取黄铜样品20g加入大烧杯中,把200g稀盐酸分四次加入,实验所得数据如表:
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸的质量/g | 50 | 50 | 50 | 50 |
剩余固体的质量/g | 16.75 | 13.5 | m | 12.2 |
分析表中数据,完成下列问题:
(1)表中m=;
(2)反应总共产生气体的质量为多少?(写出计算过程)
(3)若200g稀盐酸中HCl的质量为14.6g,其余都为水.反应结束后大烧杯中氢元素的质量为g.
