题目内容
(2010?延庆县二模)了解物质构成的微观奥秘,能帮助我们更好地认识物质变化的本质.(1)氧和硅在地壳中含量丰富,两种元素的本质区别是它们原子结构中的数不同;
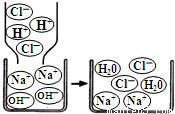
(2)如图是盐酸与氢氧化钠溶液反应的微观过程示意图.
构成氢氧化钠溶液的粒子是;
从微观粒子的角度分析,该反应的实质是.
(3)纯净物A可用作气体燃料.在一定条件下,将一定质量A与160g B按下图所示充分反应,当B反应完全时,生成132g C和72g D.
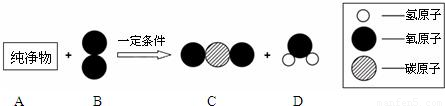
①一个B分子中含有个原子;
②A中各元素的质量比是,已知A的相对分子质量为44,该反应的化学方程式是.
③该反应的下列说法中,正确的是.
| A.属于置换反应 | B.反应前后元素种类不变 |
| C.反应前后分子数目不变 | D.反应前后原子种类、数目均不变 |
【答案】分析:(1)决定元素种类的是核电荷数(即质子数);
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子;从微观粒子的角度分析酸与碱中和的实质;
(3)根据质量守恒定律,可求A参加反应的质量;由“132gC和72gD”,结合模型图可推测C为二氧化碳,D为水,可以求出二氧化碳中的碳元素的质量,水中氢元素的质量,即A中各元素的质量比;已知A的相对分子质量为44和元素组成,可写出A的化学式,然后完成该反应的化学方程式;③根据反应的特点和化学变化的实质判断.
解答:解:(1)氧和硅在地壳中含量丰富,两种元素的本质区别是它们原子结构中的质子数不同,因为元素种类由质子数决定;
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子为Na+、OH-、H2O;从微观粒子的角度分析,该反应酸与碱中和的实质为:氢离子和氢氧根离子结合生成水分子;
(3)①B分子是氧分子,一个氧分子中含有 2个氧原子;
②由已知“将一定质量的A与160gB按下图所示充分反应,当B反应完全时,生成132gC和72gD”,根据质量守恒定律,则可求A参加反应的质量为:132+72-160=44克;结合模型图可推测C为二氧化碳,D为水,则“132gC中和72gD”二氧化碳中的碳元素的质量为132g×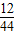 ×100%=36克,水中氢元素的质量为72g×
×100%=36克,水中氢元素的质量为72g×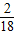 ×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2
×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2 3CO2+4H2O.③根据此反应的特点和化学反应的实质,该反应不属于置换反应,反应前后反应前后元素种类不变,原子种类、数目均不变;分子数目发生了变化;故选BD.
3CO2+4H2O.③根据此反应的特点和化学反应的实质,该反应不属于置换反应,反应前后反应前后元素种类不变,原子种类、数目均不变;分子数目发生了变化;故选BD.
故答案为:(1)质子数;
(2)钠离子、氯离子、水分子(或Na+、OH-、H2O);OH-和H+结合形成H2O分子(或氢氧根离子和氢离子结合形成水分子);
(3)①2;②m(C):m(H)=9:2;C3H8+5O2 3CO2+4H2O;③BD.
3CO2+4H2O;③BD.
点评:了解微粒观点及模型图的应用;根据质量守恒定律掌握有关原子数量的计算;掌握元素质量比的计算;能正确书写化学方程式和根据化学方程式的特点判断反应类型.
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子;从微观粒子的角度分析酸与碱中和的实质;
(3)根据质量守恒定律,可求A参加反应的质量;由“132gC和72gD”,结合模型图可推测C为二氧化碳,D为水,可以求出二氧化碳中的碳元素的质量,水中氢元素的质量,即A中各元素的质量比;已知A的相对分子质量为44和元素组成,可写出A的化学式,然后完成该反应的化学方程式;③根据反应的特点和化学变化的实质判断.
解答:解:(1)氧和硅在地壳中含量丰富,两种元素的本质区别是它们原子结构中的质子数不同,因为元素种类由质子数决定;
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子为Na+、OH-、H2O;从微观粒子的角度分析,该反应酸与碱中和的实质为:氢离子和氢氧根离子结合生成水分子;
(3)①B分子是氧分子,一个氧分子中含有 2个氧原子;
②由已知“将一定质量的A与160gB按下图所示充分反应,当B反应完全时,生成132gC和72gD”,根据质量守恒定律,则可求A参加反应的质量为:132+72-160=44克;结合模型图可推测C为二氧化碳,D为水,则“132gC中和72gD”二氧化碳中的碳元素的质量为132g×
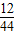 ×100%=36克,水中氢元素的质量为72g×
×100%=36克,水中氢元素的质量为72g×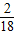 ×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2
×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2 3CO2+4H2O.③根据此反应的特点和化学反应的实质,该反应不属于置换反应,反应前后反应前后元素种类不变,原子种类、数目均不变;分子数目发生了变化;故选BD.
3CO2+4H2O.③根据此反应的特点和化学反应的实质,该反应不属于置换反应,反应前后反应前后元素种类不变,原子种类、数目均不变;分子数目发生了变化;故选BD.故答案为:(1)质子数;
(2)钠离子、氯离子、水分子(或Na+、OH-、H2O);OH-和H+结合形成H2O分子(或氢氧根离子和氢离子结合形成水分子);
(3)①2;②m(C):m(H)=9:2;C3H8+5O2
 3CO2+4H2O;③BD.
3CO2+4H2O;③BD.点评:了解微粒观点及模型图的应用;根据质量守恒定律掌握有关原子数量的计算;掌握元素质量比的计算;能正确书写化学方程式和根据化学方程式的特点判断反应类型.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
 (2010?延庆县二模)随着人们生活水平的提高,人们对于食品不但要求营养,更要求健康.市场上出现了一些不添加防腐剂的绿色食品,这种食品中有一个单独包装的保鲜剂,不会危害食品安全.某同学找来一种在空气中放置一段时间的食品保鲜剂,对它进行探究.
(2010?延庆县二模)随着人们生活水平的提高,人们对于食品不但要求营养,更要求健康.市场上出现了一些不添加防腐剂的绿色食品,这种食品中有一个单独包装的保鲜剂,不会危害食品安全.某同学找来一种在空气中放置一段时间的食品保鲜剂,对它进行探究.【查找资料】
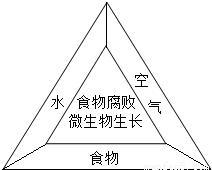
(1)食物腐败是因为微生物在食物上生长.如图所示,微生物只要得到养分,再加上充足的氧气和水,在适当的条件下就会迅速生长.因此,只要缺少一种条件,就可以防止食物腐败.
(2)常见的具有吸水性的物质有以下几种:
①浓硫酸 ②生石灰 ③氢氧化钠固体 ④铁粉
⑤硅胶(化学式SiO2?nH2O,无色透明粒状固体,无毒无害)
【活动与探究】
(3)初步探究:你认为①~⑤的物质中,不适合做食品干燥剂的是______,理由是______.
(4)实验探究:
| 实验 | 操作 | 主要现象 | 结论与解释 |
| 实验1 初步判断 | 打开这种保鲜剂的包装袋,取少量样品于试管中,进行观察. | 该样品为白色固体. | 该保鲜剂一定不是______. |
| 实验2 对该保鲜剂的有效性进行探究 | 向实验1的试管中加入适量的水,震荡. | 形成白色浑浊液体,试管壁发热. | 结论与相关反应方程式 ______. |
| 实验3 对该保鲜剂的成分进行探究 | 过滤实验2所的液体,向滤液中通入二氧化碳. | 溶液变浑浊. | 该保鲜剂中一定含有的物质是 ______,对于实验3不能确定的物质是______. |
| 将滤渣放入另一试管中,加入足量稀盐酸. | 有气泡产生. |
(5)对于实验3不能确定的物质,某同学经过仔细研究,认为直接取原固体滴加酚酞溶 液,通过观察颜色变化即可确定是否含有该物质,你认为这种方法是否合理?说明理由______.
(6)请根据食物腐败的条件分析,我们除可以使用这些保鲜剂外,还可以采用的保鲜方法是______.(写出一种即可)