题目内容
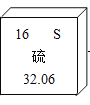
【题目】下表为元素周期表中某一周期元素的原子结构示意图。请回答下列问题:
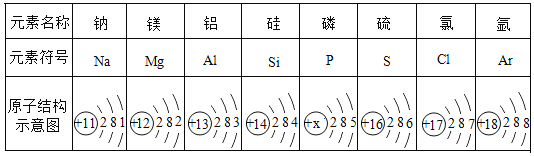
(1)表中不同种元素最本质的区别是_________(填序号):A 相对原子质量不同 B 质子数不同 C 中子数不同
(2)表中磷原子的核电荷数x=___________。
(3)镁原子在化学反应中易_______(填“得到”或“失去”)电子,形成的离子的符号是__________,说明元素的化学性质与原子的________________关系密切。镁元素属于___________(填“金属”或“非金属”)元素。
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:_____________________(填字母序号)
A 从左到右,各元素原子的电子层数相同
B 从左到右,各元素原子的原子序数依次增加
C 从左到右,各元素原子的最外层电子数相同
【答案】B 15 失去 Mg2+ 最外层电子个数 金属 AB
【解析】
(1)元素是具有相同质子数(核电荷数)的一类原子的总称,不同种元素最本质的区别是质子数不同,故选B。
(2)表中磷原子的核电荷数x=2+8+5=15。
(3)镁原子最外层有2个电子,在化学反应中易失去电子,形成的镁离子带有两个单位的正电荷,其符号是Mg2+,说明元素的化学性质与原子的最外层电子个数关系密切。汉字带金字旁的元素都属于金属元素,镁元素属于金属元素。
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,同一周期,各元素原子的电子层数相同、各元素原子的原子序数依次增加,故选AB。

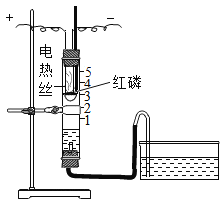
【题目】利用下图装置进行空气中氧气含量测定实验。
实验装置 | 实验操作 |
| I.向玻璃管和水槽内加适量的水,在燃烧匙里放足量红磷,塞紧塞子,上下移动水槽至两边水面相平于玻璃管的零刻度位置。 II.接通电源,待红磷燃烧,断开电源。 III.当温度恢复至室温,水不再进入玻璃管时,上下移动水槽至两边水面相平。 |
(1)实验中加入足量红磷的目的是_________。
(2)实验结束后,玻璃管内水面最终到达刻度线_______(填数字序号)处。
(3)实验操作I、III中,上下移动水槽至两边水面相平的目的是________。