题目内容
【题目】向26.4g硫酸钠和碳酸钠的混合物中滴加硫酸溶液,直到不再产生气体为止(假设气体全部逸出),共用去98g质量分数为10%的硫酸溶液.求:
(1)原混合物中碳酸钠的质量分数.
(2)反应后溶液中溶质的质量分数.
【答案】(1)原混合物中碳酸钠的质量分数为40.2%;
(2)反应后溶液中溶质的质量分数为25%.
【解析】(1)由题意,设原混合物中碳酸钠的质量为x,生成Na2SO4的质量为y,生成CO2质量为z,
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
106 98 142 44
x 98g×10% y z
![]()
x=10.6g
y=14.2g
z=4.4g
原混合物中碳酸钠的质量分数:![]() =40.2%
=40.2%
后溶液中Na2SO4的总质量为15.8g+14.2g=30 g
反应后溶液中溶质的质量分数为![]() =25%
=25%

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)右图是铝的原子结构示意图。

①下列说法不正确的是 。
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
②铝作为地壳中含量最丰富的金属,却直到19世纪末才被人类广泛应用于生活,这主要是跟铝的 有关,铝制品之所以耐腐蚀,是由于 (用化学方程式表示)。
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了右图实验,并对溶液A和固体B的成分进行了分析和实验探究。

【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2 ② Zn (NO3)2、AgNO3
③ Zn (NO3)2、Cu(NO3)2
④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是 (填标号),其理由是 ;
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现 象 | 有关反应的化学方程式 | 结论 |
取少量固体B,滴加 | 有气泡产生 | 固体B中所含金属有 |
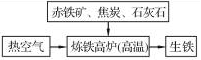
(3)右图是工业炼铁示意图。工业炼铁的设备是 ,其中,焦炭的作用是燃烧提供能量和 ;有铁生成的化学方程式为 ,炼得的铁是 (填“纯净物”或“混合物”)。
【题目】溶液在生命活动和生产、生活中都起到十分重要的作用.
(1)将下面调味品加入水中,不能形成溶液的是 .
A.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶剂为 .(写出物质名称)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
实验编号 | a | b | c | d |
加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
所得溶液的质量 | 95 | 100 | 105 | 105 |
①实验a、b、c、d中,有未被溶解的KNO3固体的实验是 (填写实验编号).
②实验a、b、c、d所得溶液中,溶质质量分数大小关系为:a<b c d(填“<”、“>”或“=”).
③取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,可以采取的操作是 .
【题目】水和溶液在生活、生产中有着重要的作用。
(1)洗衣服时发现肥皂不易产生泡沫且易起浮渣,说明所用的水是 (选填“硬水”或“软水”)。
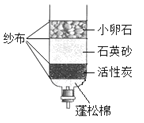
(2)右图所示的简易净水器中,小卵石、石英砂、活性炭均能起到 的作用。
(3)氯化钠在水溶液中是以 的形式存在。要把50g质量分数为9%的氯化钠溶液稀释为质量分数为0.9%的生理盐水,需要水的质量为 g。
(4)硝酸钾在不同温度时的溶解度见下表:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
下图A、B、C、D四个烧杯中分别盛有100g水,40℃时向其中分别加入110g、86g、64g、32g硝酸钾,充分溶解。
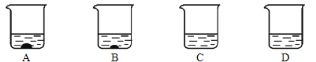
① 中的液体是饱和溶液(选填字母)。
②为了使A、B烧杯中没有溶解的固体恰好溶解,40℃时向A烧杯中加适量的水,将B烧杯中的物质升温至50℃,此时B烧杯中溶液的质量为 g,A烧杯中溶液的溶质质量分数 B烧杯中溶液的溶质质量分数(选填“>”、“=”或“<”)。