题目内容
【题目】金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)右图是铝的原子结构示意图。

①下列说法不正确的是 。
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
②铝作为地壳中含量最丰富的金属,却直到19世纪末才被人类广泛应用于生活,这主要是跟铝的 有关,铝制品之所以耐腐蚀,是由于 (用化学方程式表示)。
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了右图实验,并对溶液A和固体B的成分进行了分析和实验探究。

【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2 ② Zn (NO3)2、AgNO3
③ Zn (NO3)2、Cu(NO3)2
④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是 (填标号),其理由是 ;
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现 象 | 有关反应的化学方程式 | 结论 |
取少量固体B,滴加 | 有气泡产生 | 固体B中所含金属有 |
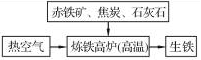
(3)右图是工业炼铁示意图。工业炼铁的设备是 ,其中,焦炭的作用是燃烧提供能量和 ;有铁生成的化学方程式为 ,炼得的铁是 (填“纯净物”或“混合物”)。
【答案】(1)①C②4Al + 3O2 ===2Al2O3
(2)【交流讨论】 ② 银的活动性比铜强,若铜被置换出来,溶液中一定没有Ag+
【实验探究】HCl Zn + 2HCl == ZnCl2 + H2↑ Zn、Cu、Ag
(3)高炉 产生还原性气体一氧化碳 3CO+ Fe2O3![]() 2Fe + 3CO2 混合物
2Fe + 3CO2 混合物
【解析】
试题分析:(1)①由图可知质子数为13;最外层电子数为3易失去形成带3个正电荷的铝离子,因此铝显+3价;铝导电性好可作导线,都正确;只有C铝是地壳中含量最多的金属元素,氧才是地壳中最多的元素,错误② 化学性质非常活泼,但铝与氧气反应会形成致密的氧化铝薄膜,隔绝空气保护铝;
(2)【交流讨论】由金属活动性顺序表的应用可知Na>Cu>Ag,AgNO3和Cu(NO3)2混合溶液中加入Zn,Zn + Cu(NO3)2 == Zn(NO3)2 + Cu,Zn + 2AgNO3 == Zn(NO3)2 + 2Ag,Cu + 2AgNO3 == Cu(NO3)2 + 2Ag。因此可简单认定Zn先与AgNO3反应,AgNO3完全反应完后再与Cu(NO3)2 反应。
综上溶质组合可以是:1、AgNO3 反应一部分Zn被消耗完,Zn(NO3)2 、AgNO3、Cu(NO3)2,
2、AgNO3 恰好反应完Zn被消耗完,Zn(NO3)2 、Cu(NO3)2,
3、AgNO3 反应完、Cu(NO3)2反应一部分Zn被消耗完,Zn(NO3)2 、Cu(NO3)2,
4、AgNO3 反应完、Cu(NO3)2反应完Zn被消耗完或者还有剩余,Zn(NO3)2。
因此不正确的为②,Zn优先与AgNO3反应。
【实验探究】若猜想①成立,那么AgNO3 反应完、Cu(NO3)2反应完Zn被消耗完或者还有剩余,固体组合可以是Cu、Ag或者Cu、Ag、Zn。现象为有气泡,那么肯定为Cu、Ag、Zn,因为只有Zn才能与酸反应生成氢气;
(3)产生还原性气体一氧化碳;为一氧化碳和氧化铁的还原反应; 生成的为生铁,含量杂质属于混合物。
