题目内容
【题目】以下为制备纳米CaCO3的一种流程:
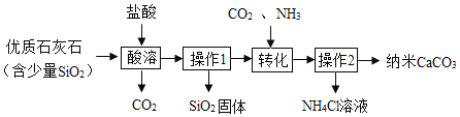
(1)“酸溶”步骤中,反应的化学方程式为_______。
(2)实验室中操作1、2名称是________,该操作中玻璃棒的作用是______。
(3)过程中的生成物可直接用于流程的是_______。
(4)为了提高转化速率,可采用的措施有___(填序号)。
a.搅拌溶液 b.适当增大通入气体的速率 c.加热溶液至100℃
(5)操作2得到的溶液,农业上可用作___。
(6)操作2所得固体还要进行以下操作:洗涤、___。检验固体已洗净的方法是:__。
【答案】CaCO3+2HCl =CaCl2+H2O+CO2↑ 过滤 引流 CO2 a、b 氮肥(或化学肥料) 干燥 取最后一次洗涤后的滤液,滴加硝酸银溶液,无现象(或取最后一次洗涤后的滤液,滴加氢氧化钠溶液并加热,没产生能使湿润的红色石蕊试纸变蓝的气体)
【解析】
(1)“酸溶”步骤中,碳酸钙和盐酸反应,反应的化学方程式为CaCO3+2HCl =CaCl2+H2O+CO2↑。
(2)实验室中操作1、2都是将固液分离,操作是过滤,玻璃棒的作用是引流。
(3)根据流程图,过程中的生成物可直接用于流程的是CO2。
(4) 搅拌溶液、适当增大通入气体的速率可以提高转化速率,由于反应在常温下进行,加热溶液至100℃对提高转化速率没有效果。
(5)操作2得到的氯化铵溶液,农业上可用作氮肥。
(6)操作2所得固体还要进行以下操作:洗涤、干燥。检验固体已洗净的方法是:取最后一次洗涤后的滤液,滴加硝酸银溶液,无现象(或取最后一次洗涤后的滤液,滴加氢氧化钠溶液并加热,没产生能使湿润的红色石蕊试纸变蓝的气体)。
故答案:(1). CaCO3+2HCl =CaCl2+H2O+CO2↑ (2). 过滤 、引流 (3). CO2 (4). a、b (5). 氮肥(或化学肥料) (6). 干燥 、取最后一次洗涤后的滤液,滴加硝酸银溶液,无现象(或取最后一次洗涤后的滤液,滴加氢氧化钠溶液并加热,没产生能使湿润的红色石蕊试纸变蓝的气体)

 名校课堂系列答案
名校课堂系列答案【题目】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯中,并敞口存放于空气中,烧杯中物质质量随时间变化如表所示,回答下列问题。
时间 | 质量/g | |||||
水 | 饱和石灰水 | 稀盐酸 | 浓硫酸 | 氯化钠浓溶液 | 氯化钙浓溶液 | |
1天 | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 5.94 | 6.69 | 12.55 | 8.47 | 10.33 |
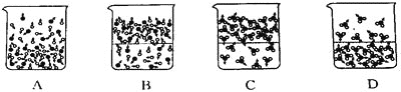
(1)下列图示能反映水在空气中放置时发生变化的微观示意图是____(填字母序号)(图中●表示氧原子,○表示氢原子)
(2)石灰水在空气中久置后有浑浊现象,其原因是(用化学方程式表示)____。
(3)为研制一种安全、环保的除湿剂,可选择上表中的____(填溶质的化学式)。
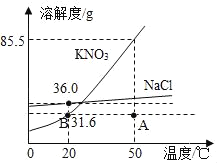
(4)将10.00g氯化钠浓溶液敞口久置后,最终得到2.26g晶体,则该溶液是____(填“饱和”或“不饱和”)溶液。(已知该温度下氯化钠的溶解度为36.1g)
(5)浓硫酸敞口久置后质量变大是因为浓硫酸具有___性。
(6)为进一步研究稀盐酸敞口久置后溶液中溶质质量分数的变化,同学们猜想溶质质量分数会变大,理由是____。