题目内容
【题目】如图是硝酸钾和氯化钠的溶解度曲线,请回答:
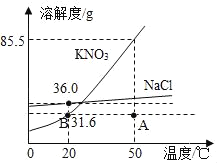
(1)50℃时,100g水中最多可以溶解_____g硝酸钾。
(2)20℃时,向100g水中加入30g硝酸钾固体,充分搅拌后,所得溶液为_____溶液(填“饱和”或“不饱和”)。
(3)硝酸钾固体中含有少量氯化钠,提纯硝酸钾的方法是_____。
(4)20℃时,将KNO3、NaCl两种物质的饱和溶液各100g,分别恒温蒸发10g水,析出晶体最多的是_____(填“KNO3”或“NaCl”)。
【答案】85.5 不饱和 溶解,蒸发浓缩,冷却结晶,过滤,洗涤,干燥 NaCl
【解析】
(1)由图可知,50 ℃时,硝酸钾溶解度为85.5 g,故50 ℃时,100 g水中最多可以溶解85.5 g硝酸钾。
(2)由图可知,20 ℃时,硝酸钾溶解度为31.6 g,故20 ℃时,向100 g水中加入30 g硝酸钾固体,充分搅拌后,所得溶液为不饱和溶液。
(3)将固体溶解,蒸发浓缩得到硝酸钾的饱和溶液,硝酸钾的溶解度随温度的变化比较大,降温硝酸钾析出,氯化钠的溶解度随温度变化不大留在溶液中,然后经过过滤、洗涤、干燥,得到硝酸钾。
(4)20 ℃时,氯化钠的溶解度大于硝酸钾的溶解度,故两种物质的饱和溶液各100 g中含溶质质量较大的是氯化钠,故分别恒温蒸发10 g水,析出晶体最多的是氯化钠。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案【题目】某同学为了研究在实验室中用某氯酸钾样品制取氧气的有关问题,他将5g氯酸钾样品与1g二氧化锰混合加热,在不同时刻测得部分数据如下表(友情提示:可把表中的空白补全后作答)。
加热时间 | t1 | t 2 | t3 | t4 |
剩余固体质量/g | 5.04 | 4.08 | ||
生成O2质量/g | 1.84 | 1.92 |
回答:
(1)t3时刻后,氯酸钾是否已经完全反应?_____。
(2)该样品中氯酸钾的质量分数_____。
(3)求t1时刻原氯酸钾中已分解的氯酸钾的质量分数____(写出解题过程)。