题目内容
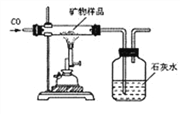
【题目】某化学兴趣小组的同学为了体验工业冶炼金属的过程,在实验室里做了用CO还原CuO的实验。他们称得装有CuO粉末的玻璃管重42 g,反应完全后,恢复到室温称量,玻璃管和固体残留物共重40.4 g,并收集到CO2 4.4 g,请你和他们一起计算:
(1) 42 g-40.4 g=l.6 g,1.6 g表示__________________的质量。
(2)该反应制得的铜的质量为__________。
【答案】 参加反应的氧化铜中氧元素 6.4 g
【解析】(1)试管与内装的氧化铜粉末共重42g,反应中氧化铜失去氧而生成铜,试管与生成的铜共重40.4g,所以固体减少量为42g-40.4g=1.6g,则1.6g表示 反应的CuO中氧元素的质量;
(2)解:设制的铜的质量为X
CO+CuO ![]() Cu+CO2
Cu+CO2
64 44
X 4.4g
![]()
X=6.4g
答:可制的铜的质量为6.4g。

【题目】三明市民新水泥厂化验室,为了测定其矿山石灰石中碳酸钙的质量分数,取石灰石样品与是量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水)。有关实验数据如下表:
反应前 | 反应后 | ||
实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
150g | 12g | 157.6g | |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为_______g。
(2)求该石灰石中碳酸钙的质量分数为__________。
【题目】生命的孕育和维系需要水,科学研究离不开水.请你完成下列探究.
探究一:用水作溶剂.在盛有5ml水和5ml汽油的两只试管中各加入1~2小粒高锰酸钾,可观察到的现象是_____,结论:同一种物质在不同溶剂中的溶解性不同.
探究二:用水区别物质.自选两种白色固体,用水区别它们,设计实验完成下表内容.
两种白色固体 | 主要操作、现象和结论 |
_____ | _____ |
探究三:溶质在水中的溶解与结晶.
【查阅资料】20℃时,五种物质的溶解度如下表.
物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 | Na2CO3 |
溶解度/g | 36.0 | 21.0 | 37.2 | 9.6 | 21.5 |
相同温度下,不同溶质同时溶解在同一溶剂中,溶解度不变.
【提出问题】20℃时,将11.7gNaCl和15.8gNH4HCO3同时放入盛有100g水的烧杯中,充分搅拌,静置,有晶体析出(温度仍为20℃).析出的晶体是什么?
【设计实验】设计方案,并进行实验.
(1)取少量晶体与熟石灰粉末混合、研磨,无明显现象.实验目的是_____.
(2)取少量晶体于试管中,加入_____,现象为_____.
【实验结论】(3)析出的晶体是_____,晶体的质量为_____g.
【实验拓展】(4)析出晶体的原因是_____.