题目内容
【题目】(1)探究影响锌与稀硫酸反应快慢的因素。反应过程中,用前10min内收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表四组实验,获得数据如下表。
实验编号 | 试剂 | 前10 min 内产生的氢气体积(mL) | |
不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
d | 纯锌 | 40 mL 30 % | 602.8 |
①比较实验a和实验b,可以得到的结论是 。
②为了研究硫酸浓度对反应快慢的影响,需比较实验 和实验 (填编号)。
③控制其他条件相同,需控制的条件是 (例举一种条件即可)。
(2)利用锌皮和稀硫酸制取氢气,并测定锌皮中锌的质量分数
制取氢气的实验操作有:
a.收集气体;
b.向锥形瓶里装锌皮;
c.连接仪器,检查装置气密性;
d.向长颈漏斗中注入稀硫酸;
e.装配仪器。
正确的操作顺序为 。
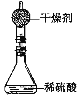
(3)测定锌皮中锌的质量分数:已知该锌皮中含有少量杂质铁,将该锌皮放入如下图所示的盛有稀硫酸的锥形瓶中,多次实验后,取平均值所得数据如下表:
反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌皮质量 | |
342.2g | 15.8g | 357.5g |
【答案】(1)①与同条件同浓度的稀硫酸反应,含杂质的锌比纯锌反应速率要快;②a和c;③温度(或者锌的颗粒的大小);(2)cbeda;(3)①0.5;②13;83.2;
【解析】
试题分析:(1)a和b中不同是纯锌和含有杂质的锌,可以看出在其他条件相同时纯锌反应慢而含有杂质的锌反应速率快;研究硫酸浓度对反应快慢的影响,就要找出其他条件相同而只有硫酸浓度不同的一组实验,故应该选用a和c进行比较;温度和固体颗粒的大小还可以影响化学反应速率,故应该控制温度要相同或者固体颗粒大小相同;(2)制取气体要先检验装置的气密性,但检验装置气密性的前提是连接好仪器;有固体和液体药品时,要先加固体药品,连接好装置后再加液体药品;最后收集气体;(3)反应中减少的质量是生成的氢气的质量;根据氢气的质量计算出锌的质量;根据锌的质量与锌皮的质量计算出锌的质量分数;

