题目内容
【题目】小明同学在理化实验考查中抽到的考题是“探究某种盐的性质”,他按照实验流程将一定质量未知白色固体溶于水配成溶液,再用贴有标号的3支试管分别取适量上述溶液,按照如图所示的方法进行试验。(氯化钙溶液呈中性)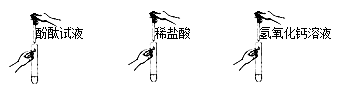
(1)实验现象:①溶液变红 ② ③产生白色沉淀
请你帮小明将实验现象补充完整。根据以上现象,小明得出结论:白色固体为碳酸钠。
(2)考试结束后,小明和小伙伴们讨论结果,发现了两个问题,他们就这两个问题请教老师,并在老师的指导下继续进行了探究实验。
问题一:白色固体一定是碳酸钠吗?
小华认为有可能是碳酸钾,小红认为还有可能是碳酸钙,小明认为小红的说法一定不对,理由是。
小明设计了方案定量研究:称取样品5.3g,加入足量的稀盐酸,产生气体的质量为2.2g。请你推断,该白色固体应为。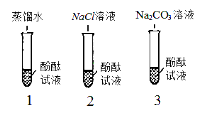
(3)问题二:碳酸钠溶液为什么能使酚酞试液变红?
【提出问题】酚酞试液变红究竟与溶液中哪种微粒有关呢?
【进行实验】同学们取了三份酚酞试液进行如图实验:
①实验1的目的是为了说明水分子不能使酚酞变红;
② 实验2的目的是为了说明;
(4)小明同学认为实验1没必要做,你认为小明的理由是;
(5)实验3滴入碳酸钠溶液,振荡,酚酞试液变红,向变红后的溶液中再滴加过量的氯化钙溶液,振荡,观察到的现象。
(6)【得出结论】酚酞试液变红与溶液中的 (填离子符号)有关。
【实验反思】若将步骤(5)中的氯化钙溶液换成石灰水,能否得出同样的结论? (填“能”或“不能”),原因是。
【答案】
(1)有气泡产生
(2)碳酸钙不溶,固体为Na2CO3
(3)Na+不能使酚酞变红
(4)NaCl溶液中有水分子
(5)产生白色沉淀,溶液由红色变成无色
(6)![]() ,不能,Ca(OH)2与Na2CO3反应能生成NaOH,溶液仍为红色
,不能,Ca(OH)2与Na2CO3反应能生成NaOH,溶液仍为红色
【解析】实验现象:滴入酚酞试液变红色,说明该盐溶液呈碱性;滴入氢氧化钙沉淀了白色沉淀,根据酸碱盐的溶解性可知该白色沉淀应是碳酸钙,故该盐含有碳酸根离子.含有碳酸根离子的物质中加入稀盐酸会产生大量的气泡,生成的是二氧化碳气体,故现象是:产生气泡;
问题一:该碳酸盐溶液能使无色酚酞变红色,那么可能是碳酸钠胡碳酸钾。由于碳酸钙难溶于水,故不可能是碳酸钙;称取样品5.3g,加入足量的稀盐酸,产生气体的质量为2.2g,即该盐与二氧化碳反应的质量比为53:22 ,碳酸钾与二氧化碳反应的质量比为138:44=69:22;碳酸钠与二氧化碳反应的质量比=106:44=53:22;故该白色固体是碳酸钠 .
【进行实验】碳酸钠溶液中含有的离子有:水分子、钠离子、碳酸根离子,可采用控制变量法来确定。②实验1的目的是为了说明水分子不能使酚酞变红;实验2加入氯化钠溶液,即加入了钠离子,酚酞不变色,说明Na+不能使酚酞变红;(4)氯化钠溶液中含有水分子、钠离子和氯离子,在氯化钠溶液中滴入酚酞试液不变红,即可说明水分子不能使无色酚酞变色,故实验1没必要做;(5)碳酸钠与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,氯化钠溶液呈中性,不能使无色酚酞变红.故能观察到的现象是产生白色沉淀,溶液由红色变成无色;【得出结论】碳酸钠溶液中含有的离子有:水分子、钠离子、碳酸根离子,水分子和钠离子均不能使无色酚酞变红,加入氯化钙溶液除去了碳酸根离子后,溶液由红色变成无色,说明酚酞试液变红与溶液中的碳酸根离子有关;【实验反思】若将步骤(5)中的氯化钙溶液换成石灰水,碳酸钠与氢氧化钙反应会生成碳酸钙沉淀和氢氧化钠,氢氧化钠呈碱性,会对实验造成干扰,故不能用石灰水代替氯化钙溶液.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室现需1.12L纯净的氧气(标准状况下,氧气的密度是1.429g/L),某同学用质量比为3:1的氯酸钾和二氧化锰制取氧气,并回收二氧化锰和氯化钾。下表为该同学实验的有关数据:
实验1.12收集L氧气后试管内固体残余物的质量 | 充分加热后试管内固体残余物的质量 |
7.98g | 6.92g |
问该同学最多能回收_______克二氧化锰?(结果精确到0.01g)