题目内容
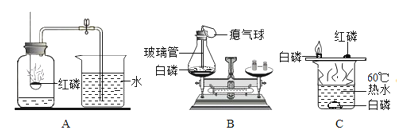
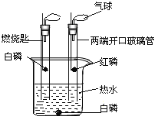
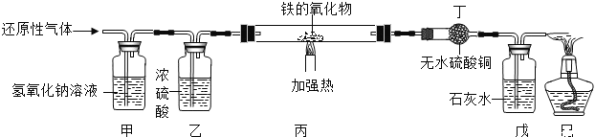
【题目】某同学模仿物理课上学到的“串联电路”,设计了如下气体制取与性质验证的组合实验。打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降并流进D中。请看图回答问题:
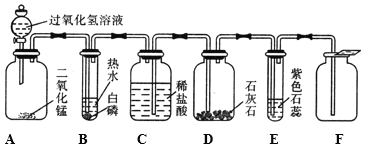
(1)A发生反应的化学方程式为______________;
(2) E中的实验现象是 _________;
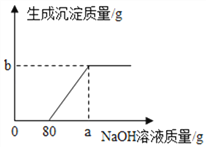
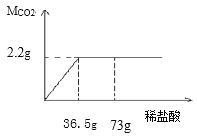
(3)现用大理石与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的质量与加入的稀盐酸的质量关系如图所示。(提示:大理石中的杂质不发生反应,气体的溶解忽略不计)求:大理石中参加反应的碳酸钙质量是__________?
【答案】2H2O2![]() 2H2O+O2↑ 紫色石蕊试液变为红色 5.0g
2H2O+O2↑ 紫色石蕊试液变为红色 5.0g
【解析】
(1)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,化学方程式为2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)C中液面下降,稀盐酸流进D中与石灰石发生反应生成二氧化碳和氯化钙,二氧化碳气体通过导管进入E装置,与紫色石蕊试液中的水发生反应生成碳酸,碳酸显酸性,可以使紫色石蕊试液变为红色;
(3)解:由图可知生成二氧化碳2.2g。设大理石中碳酸钙的质量为x,则有
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 4
x 2.2g
![]() ,得x=5.0g,故大理石中碳酸钙的质量为5.0g。
,得x=5.0g,故大理石中碳酸钙的质量为5.0g。
答:大理石中碳酸钙的质量为5.0g。

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目