��Ŀ����
40��ij�Ƽ������ˮΪ��Ҫԭ���������̼���ƣ�����������Ʒ��
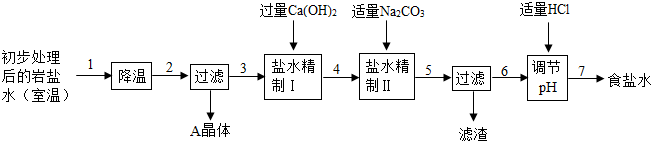
����ˮ�������������������Ƶõ�����̼��������Ҫ��ʳ��ˮ��ͬʱ��ȡ����ƷA���壬����Ҫ�������£�

��1�������¡���Ŀ������������Ʒ��A���塱��A�Ļ�ѧʽ��
��2�����������еIJ�����
��3������ˮ���Ƣ��dz�ȥ��ˮ�е������Ȼ�þ����Ӧ�Ļ�ѧ����ʽ��
��4������ˮ���Ƣ��dz�ȥ��ˮ�е��������ʣ���Ӧ�Ļ�ѧ����ʽ ��
����ˮ�������������������Ƶõ�����̼��������Ҫ��ʳ��ˮ��ͬʱ��ȡ����ƷA���壬����Ҫ�������£�

��1�������¡���Ŀ������������Ʒ��A���塱��A�Ļ�ѧʽ��
Na2SO4
����2�����������еIJ�����
����
������ʵ���ҽ��иò�������Ҫ�õ��IJ����������ձ����������⣬����©��
����3������ˮ���Ƣ��dz�ȥ��ˮ�е������Ȼ�þ����Ӧ�Ļ�ѧ����ʽ��
Ca��OH��2+MgCl2�TCaCl2+Mg��OH��2��
����4������ˮ���Ƣ��dz�ȥ��ˮ�е��������ʣ���Ӧ�Ļ�ѧ����ʽ ��
CaCl2+Na2CO3�TCaCO3��+2NaCl
����������1�����ݹ�����ܽ�����߿����жϳ����ʵ��ܽ�����¶ȱ仯�ı仯������Ӷ�ȷ��ͨ�����»��������ܼ��ķ���ʹ���ʴ���Һ�нᾧ������
��2�������Һ������ù��˵IJ��������ݹ�����Ҫ���������
��3������þ���ӵ����ʷ�������������������Һ��������������þ������ȥþ���ӣ�
��4�����ݸ����ӵ����ʷ���������̼������Һ���Ժ����ӷ�Ӧ����̼��Ƴ�������ȥ�����ӣ���д����ʽ�ؼ�Ҫ������дҪ����н��
��2�������Һ������ù��˵IJ��������ݹ�����Ҫ���������
��3������þ���ӵ����ʷ�������������������Һ��������������þ������ȥþ���ӣ�
��4�����ݸ����ӵ����ʷ���������̼������Һ���Ժ����ӷ�Ӧ����̼��Ƴ�������ȥ�����ӣ���д����ʽ�ؼ�Ҫ������дҪ����н��
����⣺��1����������ˮ��Ҫ���Ȼ��ƣ�������н϶������ƣ��Լ������Ȼ��ƺ��Ȼ�þ�������Ȼ��Ƶ��ܽ�����¶ȵ�Ӱ���С���������Ƶ��ܽ�����¶ȵĽ������Լ�С����˽���ʱ��������Ҫ��Na2SO4���ʴ�Ϊ��Na2SO4
��2�������ǰ������ľ������Һ�ֿ������Ӧ�ù��˵ķ������ʴ�Ϊ�����ˣ�©��
��3����������������Һ�ܹ�������ˮ�е��Ȼ�þ��Ӧ����������þ�������ʴ�Ϊ��Ca��OH��2+MgCl2�TCaCl2+Mg��OH��2��
��4������̼���ƺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������ʴ�Ϊ��CaCl2+Na2CO3�TCaCO3��+2NaCl
��2�������ǰ������ľ������Һ�ֿ������Ӧ�ù��˵ķ������ʴ�Ϊ�����ˣ�©��
��3����������������Һ�ܹ�������ˮ�е��Ȼ�þ��Ӧ����������þ�������ʴ�Ϊ��Ca��OH��2+MgCl2�TCaCl2+Mg��OH��2��
��4������̼���ƺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������ʴ�Ϊ��CaCl2+Na2CO3�TCaCO3��+2NaCl
������������Ҫ���������ʵķ�������ͳ�ȥ���ʵķ�����Ҫ�������ʵ�����ѡ���ʵ��ķ������Լ����н����д��ѧ����ʽʱһ��Ҫ�淶��

��ϰ��ϵ�д�
 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�
�����Ŀ
 ij�Ƽ������ˮΪ��Ҫԭ���������̼���ƣ�����������Ʒ��
ij�Ƽ������ˮΪ��Ҫԭ���������̼���ƣ�����������Ʒ����һ��ԭ������ˮ��Ҫ���Ȼ��ƣ�������н϶������ƣ��Լ������Ȼ��ƺ��Ȼ�þ���������������ڲ�ͬ�¶�ʱ���ܽ���������±���
| �¶�/�� | 0 | 10 | 20 | 30 | 40 | |
| �� | �Ȼ��� | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| �� | ������ | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 |
| �� | �Ȼ��� | 59.5 | 65.0 | 74.5 | 100 | 116 |
| /g | �Ȼ�þ | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 |
����������ˮ�������������������Ƶõ�����̼��������Ҫ��ʳ��ˮ��ͬʱ��ȡ����ƷA���壬����Ҫ�������£�
��1�������¡���Ŀ������������Ʒ��A���塱������
��2������ˮ����I���з�����Ӧ�Ļ�ѧ����ʽ��
��3������ˮ���Ƣ��з�����Ӧ�Ļ�ѧ����ʽ��
��4�������������ƹ����У�����һ�����ʲ�û���ܹ���ȫ��ȥ�������ʿ�������Һ���ƹ����в���
���������������ƺ��ʳ��ˮΪԭ�������Ĵ����Ʒ�лẬ�������Ȼ������ʣ����Ƽ��
��Ʒ��װ����ע����̼���ƺ�����96%��Ϊ�ⶨ�ò�Ʒ�к�̼���Ƶ���������������������ʵ�飺ȡ18.0g�������������ձ��У��Ƶ��ձ�����ʢ������Ʒ��������Ϊ158��Og���ٰ�lOOgϡ����ƽ���ֳ��ķ����μ�����Ʒ�У�ÿ�ξ���ַ�Ӧ��ʵ�����ݼ�¼���£�
| ��������Ĵ��� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| ��������� | 25 | 25 | 25 | 25 |
| �ձ�����ʢ���������� | 180.3 | 202.6 | 226.4 | 251.4 |
��1����һ�μ���ϡ�����ַ�Ӧ�����ɶ�����̼��������
��2���ò�Ʒ��̼���Ƶ����������Ƿ�ϸ�Ҫ��д��������̣������ȷ��0.1%��
ij�Ƽ������ˮΪ��Ҫԭ���������̼���ƣ�����������Ʒ��
��һ��ԭ������ˮ��Ҫ���Ȼ��ƣ�������н϶������ƣ��Լ������Ȼ��ƺ��Ȼ�þ���������������ڲ�ͬ�¶�ʱ���ܽ���������±���
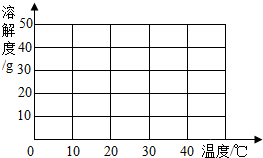
��1���������ṩ���ܽ�����ݣ����������Ƶ��ܽ�����ߣ�
��2��10��ʱ��100gˮ���Ƶõ��ı�����������Һ�����ʵ������� g�����ʵ����������� ����ȷ��0.1%����
����������ˮ�������������������Ƶõ�����̼��������Ҫ��ʳ��ˮ��ͬʱ��ȡ����ƷA���壬����Ҫ�������£�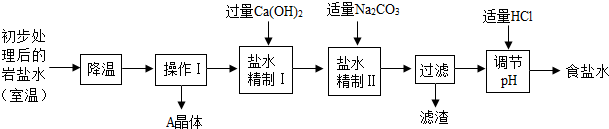
��3�������¡���Ŀ������������Ʒ��A���塱��A�Ļ�ѧʽ�� ��
��4��������I���еIJ����� ������ʵ���ҽ��иò�������Ҫ�õ��IJ����������ձ����������⣬���� ��
��5������ˮ����I���dz�ȥ��ˮ�е������Ȼ�þ����Ӧ�Ļ�ѧ����ʽ�� ��
��6������ˮ���Ƣ��dz�ȥ��ˮ�е��������ʣ���Ӧ�Ļ�ѧ����ʽ�� ��
��һ��ԭ������ˮ��Ҫ���Ȼ��ƣ�������н϶������ƣ��Լ������Ȼ��ƺ��Ȼ�þ���������������ڲ�ͬ�¶�ʱ���ܽ���������±���
| �¶�/�� | 0 | 10 | 20 | 30 | 40 | |
| �ܽ��/g | �Ȼ��� | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| ������ | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| �Ȼ��� | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| �Ȼ�þ | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
��2��10��ʱ��100gˮ���Ƶõ��ı�����������Һ�����ʵ�������
����������ˮ�������������������Ƶõ�����̼��������Ҫ��ʳ��ˮ��ͬʱ��ȡ����ƷA���壬����Ҫ�������£�

��3�������¡���Ŀ������������Ʒ��A���塱��A�Ļ�ѧʽ��
��4��������I���еIJ�����
��5������ˮ����I���dz�ȥ��ˮ�е������Ȼ�þ����Ӧ�Ļ�ѧ����ʽ��
��6������ˮ���Ƣ��dz�ȥ��ˮ�е��������ʣ���Ӧ�Ļ�ѧ����ʽ��
 ij�Ƽ������ˮΪ��Ҫԭ���������Na2CO3������������Ʒ��
ij�Ƽ������ˮΪ��Ҫԭ���������Na2CO3������������Ʒ��
