题目内容
 某制碱厂以岩盐水为主要原料生产纯碱(Na2CO3)和其他副产品.
某制碱厂以岩盐水为主要原料生产纯碱(Na2CO3)和其他副产品.(一)有关资料
原料岩盐水主要是含NaCl,此外还含有较多Na2SO4,以及少量CaCl2和MgCl2.
上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶 解 度 /g |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2SO4 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| CaCl2 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| MgCl2 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
8.8%
8.8%
(精确到0.1%).(二)生产工艺

(2)“降温”的目的是析出副产品“A晶体”,A的化学式是
Na2SO4
Na2SO4
;(3)反应器中的反应为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl.再将NaHCO3晶体转移出来后,加热所得固体即为工业纯碱.在整个生产工艺中没有涉及到的基本反应类型是
置换反应
置换反应
,可重复利用的是CO2(或NaCl)
CO2(或NaCl)
(水除外,只需一种);(4)在反应器中总是先通氨气,后通二氧化碳,原因是
因为氨气溶解度大,形成碱性环境便于二氧化碳溶解
因为氨气溶解度大,形成碱性环境便于二氧化碳溶解
.(三)工业纯碱中杂质的判断:
(5)已知:NH4Cl NH3↑+HCl↑
实验步骤:
①取一定质量的纯碱样品,经多次充分加热后再称重,发现质量无变化;
②另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
由上述实验可确定纯碱样品含有杂质
NaCl
NaCl
(写化学式).(四)含量测定
(6)称取纯碱样品21.3g于烧杯中,加入适量水将其溶解,然后逐滴加入溶质质量分数为14.6%的稀盐酸并不断用玻璃棒搅拌.先发生反应:Na2CO3+HCl=NaHCO3+NaCl;后发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑.在上述过程中烧杯中溶液质量与加入稀盐酸质量的关系如图所示(不考虑CO2的溶解),请你根据图甲提供的信息计算检测过程中产生CO2的质量
8.8g
8.8g
.(7)请通过计算并结合表判断此纯碱样品等级为
优等
优等
品.| 工业纯碱标准(Na 2CO3%≥) | ||
| 优等品 | 一等品 | 合格品 |
| 99.2 | 98.8 | 98.0 |
分析:(1)根据10℃时,Na2SO4的溶解度计算饱和Na2SO4溶液中溶质的质量分数;
(2)根据NaCl、Na2SO4、CaCl2、MgCl2的溶解度随温度的变化情况分析;
(3)根据在整个生产工艺中涉及到的反应及反应的类型分析未涉及到的反应,根据整个生产工艺分析可重复利用的物质;
(4)根据氨气易溶于水形成氨水显碱性,与二氧化碳溶于水形成的碳酸反应分析;
(5)根据氯离子的检验方法分析;
(6)根据图象分析能产生二氧化碳的盐酸的质量,有盐酸的质量求出二氧化碳的质量;
(7)要判断此纯碱样品等级,就要计算碳酸钠的质量分数,需要求得碳酸钠的质量.
(2)根据NaCl、Na2SO4、CaCl2、MgCl2的溶解度随温度的变化情况分析;
(3)根据在整个生产工艺中涉及到的反应及反应的类型分析未涉及到的反应,根据整个生产工艺分析可重复利用的物质;
(4)根据氨气易溶于水形成氨水显碱性,与二氧化碳溶于水形成的碳酸反应分析;
(5)根据氯离子的检验方法分析;
(6)根据图象分析能产生二氧化碳的盐酸的质量,有盐酸的质量求出二氧化碳的质量;
(7)要判断此纯碱样品等级,就要计算碳酸钠的质量分数,需要求得碳酸钠的质量.
解答:解:(1)由表中的数据可知,在10℃时,Na2SO4的溶解度是9.6g,饱和Na2SO4溶液中溶质的质量分数是:
×100%=8.8%;
(2)由表中的数据可知,Na2SO4的溶解度随温度的升高变化最大,所以在降温时.析出晶体最多的A是Na2SO4;
(3)由生产工艺可知,在精制盐水Ⅰ中氢氧化钙与氯化镁反应:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2,该反应属于复分解反应;反应器中的反应为:NH3+CO2+H2O=NH4HCO3,反应为化合反应.加热碳酸氢钠制取纯碱的化学方程式:2NaHCO3
Na2CO3+H2O+CO2↑属于分解反应,所以.没有涉及到的反应是置换反应,由生产工艺可知CO2、NaCl可以重复使用;
(4)在反应器中总是先通氨气,后通二氧化碳,原因是:因为氨气易溶与水,形成碱性环境便于二氧化碳溶解;
(5)由向少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.可确定纯碱样品含有杂质NaCl;
(6)根据据图甲可以看出,当加入盐酸的量为50g时开始产生二氧化碳,当加入盐酸的量为100g时不再生成二氧化碳,设产生二氧化碳的质量为x,则有
NaHCO3+HCl=NaCl+H2O+CO2↑.
36.5 44
50g×14.6% x
36.5:50g×14.6%=44:x
解得,x=8.8g
(7)根据题意可以看出,与碳酸钠反应的盐酸共有100g,设碳酸钠的质量为y,则有
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73
y 100g×14.6%
106:y=73:100g×14.6%
解得,y=21.2g,
所以该样品中纯碱的质量分数为:
×100%=99.5%>99.28%,属于优等品
故答为:(1)8.8%;(2)Na2SO4;(3)置换反应,CO2(或NaCl);(4)氨气易溶与水,形成碱性环境便于二氧化碳溶解;(5)NaCl;(6)8.8g;(7)优等.
| 9.6g |
| 100g+9.6g |
(2)由表中的数据可知,Na2SO4的溶解度随温度的升高变化最大,所以在降温时.析出晶体最多的A是Na2SO4;
(3)由生产工艺可知,在精制盐水Ⅰ中氢氧化钙与氯化镁反应:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2,该反应属于复分解反应;反应器中的反应为:NH3+CO2+H2O=NH4HCO3,反应为化合反应.加热碳酸氢钠制取纯碱的化学方程式:2NaHCO3
| ||
(4)在反应器中总是先通氨气,后通二氧化碳,原因是:因为氨气易溶与水,形成碱性环境便于二氧化碳溶解;
(5)由向少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.可确定纯碱样品含有杂质NaCl;
(6)根据据图甲可以看出,当加入盐酸的量为50g时开始产生二氧化碳,当加入盐酸的量为100g时不再生成二氧化碳,设产生二氧化碳的质量为x,则有
NaHCO3+HCl=NaCl+H2O+CO2↑.
36.5 44
50g×14.6% x
36.5:50g×14.6%=44:x
解得,x=8.8g
(7)根据题意可以看出,与碳酸钠反应的盐酸共有100g,设碳酸钠的质量为y,则有
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73
y 100g×14.6%
106:y=73:100g×14.6%
解得,y=21.2g,
所以该样品中纯碱的质量分数为:
| 21.2g |
| 21.3g |
故答为:(1)8.8%;(2)Na2SO4;(3)置换反应,CO2(或NaCl);(4)氨气易溶与水,形成碱性环境便于二氧化碳溶解;(5)NaCl;(6)8.8g;(7)优等.
点评:本题难度较大,主要考查了物质的分离操作和除去杂质的方法,要根据物质的性质选择适当的方法进行解答,培养学生对知识的应用和理解的能力;在书写化学方程式及计算过程一定要规范.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
 某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶 | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 解 | 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 |
| 度 | 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 |
| /g | 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 |
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:
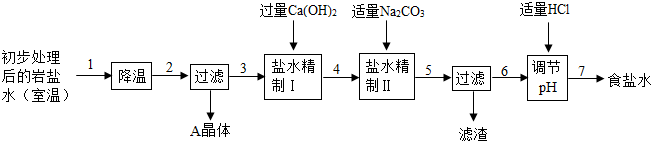
(1)“降温”的目的是析出副产品“A晶体”,它是
(2)“盐水精制I”中发生反应的化学方程式是
(3)“盐水精制Ⅱ中发生反应的化学方程式是
(4)经过上述精制过程中,仍有一种物质并没有能够完全除去,该物质可以在溶液精制过程中步骤
(三)用上述精制后的食盐水为原料生产的纯碱产品中会含有少量氯化钠杂质.该制碱厂的
产品包装袋上注明:碳酸钠含量≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取18.0g纯碱样晶放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.Og,再把lOOg稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量 | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量 | 180.3 | 202.6 | 226.4 | 251.4 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品.
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
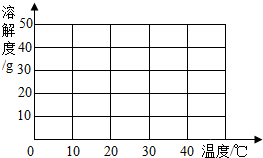
(1)根据所提供的溶解度数据,画出硫酸钠的溶解度曲线.
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是 g,溶质的质量分数是 (精确到0.1%).
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下: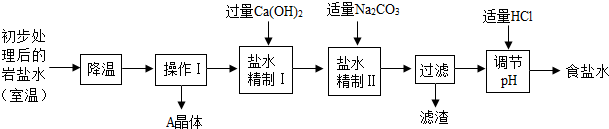
(3)“降温”的目的是析出副产品“A晶体”,A的化学式是 .
(4)“操作I”中的操作是 ,若在实验室进行该操作,需要用到的玻璃仪器除烧杯、玻璃棒外,还有 .
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是 .
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是 .
(一)原料岩盐水主要含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和氯化镁.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 硫酸钠 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| 氯化镁 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制取副产品A晶体,其主要流程如下:

(3)“降温”的目的是析出副产品“A晶体”,A的化学式是
(4)“操作I”中的操作是
(5)“盐水精制I”是除去盐水中的少量氯化镁,反应的化学方程式是
(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式是

