题目内容
【题目】北京时间2018年12月8日凌晨2时23分,中国在西昌卫星发射中心用长征三号乙载火箭成功发射嫦娥四号探测器,开启中国月球探测的新旅程。据报道:载人宇宙飞船或潜水艇中般都要安装盛放过氧化钠(Na2O2)颗粒的装置,其中过氧化钠可作供氧剂。某化学兴趣小组感到非常好奇,设计实验进行探究。
(提出问题)过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
(查阅资料)①人呼出的气体中主要成分是N2、O2、CO2和水蒸气等。
②NaOH吸收CO2效果更好:![]() 。
。
(提出猜想)过氧化钠与人呼出的N2或CO2或__________反应并生成氧气。
(进行实验)
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。
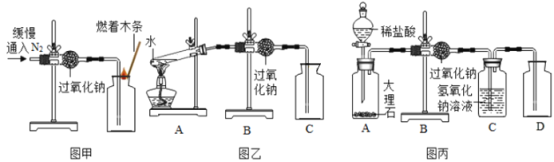
(1)实验装置如图甲所示。
(2)实验现象及结论:观察到___________现象,判断过氧化钠与氮气没有发生反应。
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
(1)同学们在老师的指导下设计了如图乙所示装置。A装置的作用是_________,发生的变化是_______变化。
(2)实验现象及结论:带火星的木条复燃;过氧化钠与水蒸气发生反应并生成氧气。
(3)若该反应还产生了氢氧化钠,请你写出化学方程式___________。
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。
(1)同学们在老师的指导下设计了如图丙所示装置。C装置的作用是___________。
(2)实验现象及结论:带火星的木条复燃;过氧化钠与二氧化碳发生反应并生成氧气。
(3)某同学对实验Ⅲ的设计提岀疑问:认为该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是_____________。
【答案】水蒸气 燃着木条熄灭 提供水蒸气 物理 ![]() 除去(吸收)CO2气体 制得的二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气
除去(吸收)CO2气体 制得的二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气
【解析】
[提出猜想]因为人呼出的气体中主要成分是N2、O2、CO2和水蒸气等,所以过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气;
故填:水蒸气。
[进行实验]实验Ⅰ:(2)该实验是把氮气通入试管中,并用集气瓶收集气体,再把燃着的木条放到集气瓶口,最终得到的结论是过氧化钠与氮气没有发生反应,所以集气瓶中收集到的是氮气,最终从瓶口逸出的也是氮气,氮气不支持燃烧,燃着的木条熄灭;
故填:燃着木条熄灭。
实验Ⅱ:(1)图乙所示的实验是验证水蒸气是否与过氧化钠反应,A装置用酒精灯加热试管中的水,水沸腾时,产生水蒸气,没有生成其他物质,是物理变化;
故填:提供水蒸气 物理变化。
(3)由该实验得到过氧化钠与水蒸气反应生成氢氧化钠和氧气,反应的化学方程式是![]() ;
;
故填:![]() 。
。
实验Ⅲ:(1)C装置里装的是氢氧化钠溶液,氢氧化钠能与二氧化碳反应,所以C装置的作用是吸收氧气中的CO2气体(或除去CO2);
故填:除去(吸收)CO2气体。
(3)在实验Ⅲ中,A装置是大理石和稀盐酸反应制取二氧化碳气体,所生成的气体中含有水蒸气,水蒸气与过氧化钠也会反应生成氧气,故他们认为该实验不能证明二氧化碳与过氧化钠确实发生了反应;
故填:制得的二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气。

 导学全程练创优训练系列答案
导学全程练创优训练系列答案【题目】探究物质燃烧。巴黎圣母院大火造成的重大损失再次提醒人们,合理的控制燃烧非常重要,小明利用下列装置对物质燃烧进行探究,探究过程和观察记录如下:
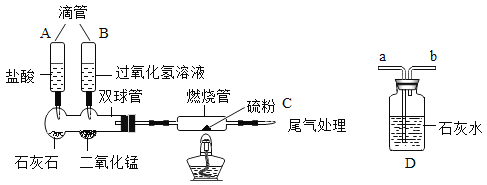
实验①:根据装置图组装仪器,不点燃酒精灯,观察到硫不燃烧。
实验②:点燃酒精灯,观察到硫燃烧,发出微弱的淡蓝色的火焰。
实验③:更换燃烧管(装有等量硫粉),挤压滴管A,在尾气处理接口接上D装置,观察到溶液变浑浊后,点燃酒精灯,硫粉不燃烧。
实验④:更换燃烧管(装有等量硫粉),拆除D装置,挤压滴管B点燃酒精灯,硫粉燃烧发出明亮的蓝紫色火焰
(1)上述实验中的对照实验(填实验编号)和获得的相应结论。
第1组对照实验:_________,结论:__________。
第2组对照实验:_________,结论:__________。
第3组对照实验:_________,结论:__________。
(2)实验③中需待D中溶液变浑浊后再点燃酒精灯,其原因是________________。
(3)写出上述实验中发生化学反应的方程式___________________(不包括处理尾气的反应)
(4)有一种吹不灭的蜡烛,点燃后任你怎么吹也吹不灭。
(查阅资料)该蜡烛芯上包裹一层打火石的粉末。打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃。当蜡烛燃烧时,金属并不燃烧;但当蜡触吹灭后,未冷却的金属发生燃烧,从而使蜡触复燃。蜡烛燃烧时金属不燃烧的原因是__________;试再举一例运用此原理灭火的生活事例_______________。
(实验探究)吹不灭的蜡烛芯内的金属可能是镁、铁或铜中的一种,为确定该金属的成分,请你自选试剂继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
操作步骤 | 现象 | 结论 |
切开蜡烛,取出打火机,用砂纸打磨 | 打火石是银白色 | __________ |
取少量打磨后的打火石于试管中,__________ | ____________ | 该金属是镁 |
在上述探究触芯内金属成分的过程中,运用的科学方法有_______________。
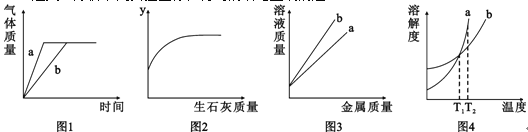
【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中然烧的实验(如图1)。

(1)根据镁燃烧发出耀眼的白光这一特点,在军事上用于制造_____;
(2)同学们通过称量发现:即使不考虑参加反应的氧气的质量,在石棉网上收集到产物的质量也小于烧掉镁条的质量,看似该反应不遵循质量守恒定律。请你分析出现这种结果的原因可能是:_____;
(3)小红按图2装置进行实验,结果符合质量守恒定律,同时还发现产物中有少量黄色固体。决定探究黄色固体为何物。

(提出问题)黄色固体是什么?
(查阅资料)得到如下信息①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体:③氮化镁可与水剧烈反应产生氨气;④氨气有刺激性气味,能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体可能是Mg3N2;
(实验探究)请设计实验,验证猜想:
实验操作 | 实验现象 | 结论 |
_____ | _____ | 黄色固体是Mg3N2 |
(反思交流)
①写出镁条燃烧生成氮化镁的化学方程式为_____;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是_____。
③氢气也可以在氯气中能够燃烧,反应方程式为 。结合以上事实,请你谈一谈对燃烧的新认识_____。
。结合以上事实,请你谈一谈对燃烧的新认识_____。