题目内容
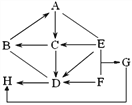
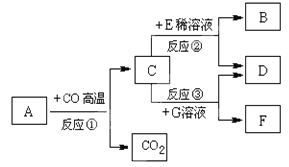
【题目】金属及金属材料在生产、生活中有广泛的应用,认识金属的性质有利于我们更好地利用金属。金属元素在自然界中分布很广,地壳中含量最多的金属元素是_______ (填“符号”)。铁钉在初中化学试验中多次出现,下图展示了光亮铁钉的一些列变化。
![]()
Ⅰ.变化①中发生反应的化学方程式是____________ 。
Ⅱ.变化②中,铁钉主要与空气中____________ 发生反应。
Ⅱ.变化③中除去铁锈的化学方程式为____________ 。
ⅲ.如果用a、b、c分别代表光亮铁钉、锈蚀铁钉、无锈铁钉,则它们的质量由大到小的顺序为____(用字母表示)
【答案】 Al ![]() O2、H2O
O2、H2O ![]() b>a>c
b>a>c
【解析】(1) Ⅰ.变化①中,铁和硫酸铜反应生成硫酸亚铁和铜,发生反应的化学方程式是:Fe+CuSO4═FeSO4+Cu;Ⅱ.变化②中,铁钉主要与空气中的水和氧气发生反应;Ⅲ.变化③中除去铁锈时,氧化铁能和稀盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;Ⅳ.光亮铁钉和水、氧气反应后得到锈蚀铁钉,因此光亮铁钉质量小于锈蚀铁钉质量,除去铁锈后得到无锈铁钉,因此无锈铁钉质量小于光亮铁钉质量,则它们的质量由大到小的顺序为b>a>c。

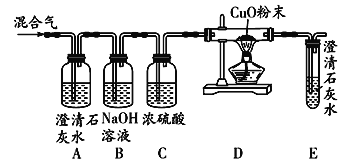
【题目】某化学兴趣小组用下图所示装置完成木炭还原氧化铜的实验,并对生成的红色固体成分进行探究。
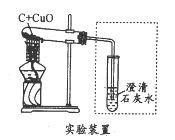
【提出问题】木炭与氧化铜反应生成的红色固体中含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O);氧化亚铜是红色固体,能与稀硫酸反应: ![]() 。
。
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
全部是铜;②全部是氧化亚铜;③是两者的混合物。
【实验探究】(1)用上图所示装置完成木炭还原氧化铜的实验,观察到澄清石灰水_______。试管冷却后,观察到黑色固体全部变为红色,对生成的红色固体成分进行探究:
实验探究
步骤 | 现象 | 结论 |
①取1.8g红色固体于试管中,滴加足量___________ ,充分反应 | ___________ | 猜想①错误 |
②过滤,将滤渣洗涤、干燥、称量 | 所得固体质量大于_______________ 克 | 猜想③正确 |