题目内容
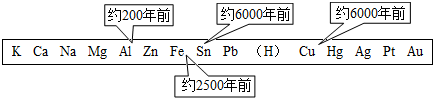
金属是一类重要的材料,人类的生活和生产都离不开金属.下图表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.

(1)根据图中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关
①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性 ④金属的延展性 ⑤金属冶炼的难易程度
(2)铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因是什么?
(3)小娟想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和必要的仪器.
①你认为她能测出铜的质量分数的合金是
②小娟取该合金的粉末32.5g,与足量该盐酸充分反应后,经测定产生了0.4g气体,请你帮助她计算出该合金中铜的质量分数?

(1)根据图中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关
③⑤
③⑤
.①地壳中金属元素的含量 ②金属的导电性 ③金属的活动性 ④金属的延展性 ⑤金属冶炼的难易程度
(2)铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因是什么?
(3)小娟想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和必要的仪器.
①你认为她能测出铜的质量分数的合金是
Cu-Zn
Cu-Zn
合金.②小娟取该合金的粉末32.5g,与足量该盐酸充分反应后,经测定产生了0.4g气体,请你帮助她计算出该合金中铜的质量分数?
分析:(1)根据已有的金属的知识进行分析,金属的活动性越强,冶炼的程度越难,利用的越晚;
(2)铝的活动性比铁强,但比铁耐腐蚀,要从形成保护膜角度考虑;
(3)根据在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气分析;根据生成氢气的质量,可以求得合金中锌的质量,从而求得铜的质量和铜的质量分数.
(2)铝的活动性比铁强,但比铁耐腐蚀,要从形成保护膜角度考虑;
(3)根据在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气分析;根据生成氢气的质量,可以求得合金中锌的质量,从而求得铜的质量和铜的质量分数.
解答:解:(1)由题可知地壳里含量最高的是金属铝,但铝开发利用的时间在后,说明金属大规模开发、利用的先后顺序与地壳里金属含量无关,同时与金属的导电性和延展性也无关,而是与金属活动性顺序和金属冶炼的难易程度有关:金属的活动性越强,冶炼的程度越难,利用的越晚;故选③⑤;
(2)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,是因为铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性.
故答案为:铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性;
(3)①只给出盐酸和必要的仪器,则合金中需含有能与盐酸反应的金属,锌排在氢的前面,而铜和银排在氢的后面,不与盐酸反应,所以只能测出铜锌合金.
故本题答案为:Cu~Zn;
②设生成0.4g氢气需要锌的质量为x,则有
Zn+2HCl═ZnCl2+H2↑
65 2
x 0.4g
=
解之得:x=13g
该合金中的Cu的质量分数是=
×100%=60%.
故该合金中铜的质量分数为60%.
(2)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,是因为铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性.
故答案为:铝容易与空气中的氧气发生反应,会生成一层致密的氧化铝膜覆盖在铝的表面,阻止反应的进行,所以具有良好的抗腐蚀性;
(3)①只给出盐酸和必要的仪器,则合金中需含有能与盐酸反应的金属,锌排在氢的前面,而铜和银排在氢的后面,不与盐酸反应,所以只能测出铜锌合金.
故本题答案为:Cu~Zn;
②设生成0.4g氢气需要锌的质量为x,则有
Zn+2HCl═ZnCl2+H2↑
65 2
x 0.4g
| 65 |
| X |
| 2 |
| 0.4g |
解之得:x=13g
该合金中的Cu的质量分数是=
| 32.5g-13g |
| 32.5g |
故该合金中铜的质量分数为60%.
点评:本题从金属的利用,锈蚀等方面全面考查了金属的性质,本题考查了金属活动顺序的运用以及根据化学方程式进行的计算,在解第二问时要注意解题的规范性.

练习册系列答案
相关题目


 金属是一类重要的材料,人类的生活和生产都离不开金属.
金属是一类重要的材料,人类的生活和生产都离不开金属.