题目内容
水和溶液在生命活动和生活中起着十分重要的作用。根据下面的溶解度表与溶解度曲线,回答下列问题:

|
温度/°C 溶解度/g |
0 |
20 |
40 |
60 |
80 |
|
KNO3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
|
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
|
Ca(OH)2 |
0.173 |
0.165 |
0.121 |
0.116 |
0.094 |
(1)A是 的溶解度曲线。
(2)若用溶质质量分数为10%的NaCl溶液来配制100g溶质质量分数为0.9%的氯化钠溶液,需加水 g。
(3)硝酸钾中混有少量的氯化钠,想要得到纯净的硝酸钾的方法是 。
(4)60℃时,向两个分别盛有50g NaCl和KNO3的烧杯中,各加入100g的水,充分溶解后为饱和溶液的是 溶液;将上述烧杯中剩余固体全部溶解,变为不饱和溶液,下列方法能实现的是 (填序号)。
A.升温 B.加入该溶质 C.加入适量水
D.降温 E.加入足量该溶质的不饱和溶液
(5)如右图所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,原因是 。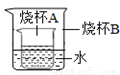
(1)硝酸钾 (2)91 (3)降温结晶法或冷却热饱和溶液 (4)NaCl C E
(5)生石灰与与水反应放热,使氢氧化钙溶解度减小而析出
【解析】
试题分析:(1)根据溶解度曲线和表格可知,A曲线的溶解度随温度上升而增大,且变化最快,所以A是硝酸钾;(2)100g溶质质量分数为0.9%的氯化钠溶液中含氯化钠质量为0.9g,稀释前后溶质质量不变,所以稀释前溶液质量为 ,需加水的质量为100g-9g=91g;(3)硝酸钾溶液溶解度随温度变化较大,氯化钠溶解度随温度变化较小,所以硝酸钾中混有少量的氯化钠,可以采用降温结晶法或冷却热饱和溶液法提纯硝酸钾;(4)60℃时,硝酸钾的溶解度为110g,氯化钠的溶解度为37.3g,也就是说此温度下100g水中最多可以溶解110g硝酸钾、37.3g氯化钠,充分溶解后为饱和溶液的是氯化钠溶液,加入适量水或者加入足量该溶质的不饱和溶液都可以将上述烧杯中剩余固体全部溶解,变为不饱和溶液;(5)生石灰与与水反应放热,使氢氧化钙溶解度减小而析出,所以变浑浊。
,需加水的质量为100g-9g=91g;(3)硝酸钾溶液溶解度随温度变化较大,氯化钠溶解度随温度变化较小,所以硝酸钾中混有少量的氯化钠,可以采用降温结晶法或冷却热饱和溶液法提纯硝酸钾;(4)60℃时,硝酸钾的溶解度为110g,氯化钠的溶解度为37.3g,也就是说此温度下100g水中最多可以溶解110g硝酸钾、37.3g氯化钠,充分溶解后为饱和溶液的是氯化钠溶液,加入适量水或者加入足量该溶质的不饱和溶液都可以将上述烧杯中剩余固体全部溶解,变为不饱和溶液;(5)生石灰与与水反应放热,使氢氧化钙溶解度减小而析出,所以变浑浊。
考点:溶解度曲线的意义
点评:关于溶解度曲线的题目一直是中考的必考点,常在双选中出现,得分率不是很高,注意仔细审题,避免粗心。

 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案(6分)水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)净水器中经常使用活性炭,主要利用活性炭的_______性。
(2)根据图中实验只生成了氢气和氧气,确定水是由氢元素和氧元素组成的,得到此结论的依据是________。写出此实验中发生反应的化学方程式________。
(3)烧杯中盛有一定质量、温度为80℃、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量。测定结果记录如下表。
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体M的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
① 65℃时,该溶液是否为饱和溶液? (填“是”、“否”或“无法判断”);
②将t℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的的是 (填字母序号);
A. 升温 B. 降温 C. 加溶质M
D. 加水 E. 加另一种固体N F. 恒温蒸发水
G. 与t℃时M的饱和溶液混合
③ 20℃时,用固体粉末M和水配制100g溶质质量分数为5%的M溶液,必须用到的仪器有:托盘天平(带砝码)、烧杯、 。
 (2013?通州区一模)水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与溶解度曲线(图1),回答下列问题:
(2013?通州区一模)水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与溶解度曲线(图1),回答下列问题:

 (2012?昌平区二模)水和溶液在生命活动和生产、生活中起着十分重要的作用.
(2012?昌平区二模)水和溶液在生命活动和生产、生活中起着十分重要的作用.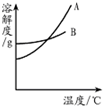 水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与
水和溶液在生命活动和生活中起着十分重要的作用.根据下面的溶解度表与