题目内容
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验,取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀H2SO4反应,都生成+2价金属的硫酸盐,反应情况如图所示,下列对该图象理解的叙述中,正确的是( )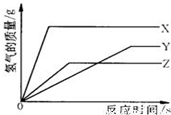
A.金属活动性由强到弱为Z、X、Y
B.金属活动性由强到弱为X、Y、Z
C.X、Y、Z依次可能是Mg、Zn、Fe
D.相对原子质量的大小为Z>Y>X
【答案】分析:“足量稀硫酸”,等质量的三种金属完全反应,放出氢气的质量= ×金属质量;
×金属质量;
根据相同时间内放出氢气的多少判断反应速率快慢,再利用反应速率判断金属活动性强弱.
解答:解:A、据图可以看出,X的斜线最陡,反应的速率最快,Y的斜线最平缓,故的速率最慢,故其活动性为X>Z>Y,故A错误;
B、据图可以看出,X的斜线最陡,反应的速率最快,Y的斜线最平缓,故Y的速率最慢,故B错误;
C、在金属活动性顺序中,Mg>Zn>Fe,不符合其活动性为X>Z>Y,故C错误;
D、等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,则金属的相对原子质量越大,反应生成氢气的质量越少,故D正确;
故选D.
点评:质量相等的金属与足量酸完全反应放出氢气的多少与金属的相对原子质量成反比,与金属的化合价相成正比.
 ×金属质量;
×金属质量;根据相同时间内放出氢气的多少判断反应速率快慢,再利用反应速率判断金属活动性强弱.
解答:解:A、据图可以看出,X的斜线最陡,反应的速率最快,Y的斜线最平缓,故的速率最慢,故其活动性为X>Z>Y,故A错误;
B、据图可以看出,X的斜线最陡,反应的速率最快,Y的斜线最平缓,故Y的速率最慢,故B错误;
C、在金属活动性顺序中,Mg>Zn>Fe,不符合其活动性为X>Z>Y,故C错误;
D、等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,则金属的相对原子质量越大,反应生成氢气的质量越少,故D正确;
故选D.
点评:质量相等的金属与足量酸完全反应放出氢气的多少与金属的相对原子质量成反比,与金属的化合价相成正比.

练习册系列答案
相关题目
 19、某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z粉末分别与足量的溶质质量分数相同的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况用右图来表示.下列顺序正确的是
19、某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z粉末分别与足量的溶质质量分数相同的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况用右图来表示.下列顺序正确的是 (2005?白下区一模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如右图所示.下列对该图象理解的叙述中,正确的是( )
(2005?白下区一模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如右图所示.下列对该图象理解的叙述中,正确的是( ) (2008?怀柔区二模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况用如图来表示.下列对该图象理解的叙述中,正确的是( )
(2008?怀柔区二模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况用如图来表示.下列对该图象理解的叙述中,正确的是( )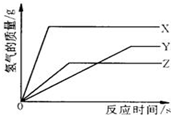 某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验,取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀H2SO4反应,都生成+2价金属的硫酸盐,反应情况如图所示,下列对该图象理解的叙述中,正确的是( )
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验,取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀H2SO4反应,都生成+2价金属的硫酸盐,反应情况如图所示,下列对该图象理解的叙述中,正确的是( )