题目内容
【题目】![]() 是常见的7种物质,其中A为黑色固体,
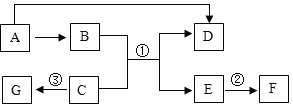
是常见的7种物质,其中A为黑色固体,![]() 为单质,B是易与血红蛋白结合的有毒气体,B、D的组成元素相同,反应①是工业用赤铁矿炼铁的主要反应,F为红色固体,G为黄色溶液。(部分反应条件已略去)。请回答下列问题:
为单质,B是易与血红蛋白结合的有毒气体,B、D的组成元素相同,反应①是工业用赤铁矿炼铁的主要反应,F为红色固体,G为黄色溶液。(部分反应条件已略去)。请回答下列问题:
(1)写出物质D的化学式:________。
(2)反应②的现象是:________________。
(3)反应③的化学方程式:________。(只写一种)
【答案】CO2 铁的表面有红色固体生成,溶液由蓝色变成浅绿色 Fe2O3+6HCl = 2FeCl3+3H2O或Fe2O3+3H2SO4= Fe 2(SO4)3+3H2O。
【解析】
是常见的7种物质,其中A为黑色固体,![]() 为单质,B是易与血红蛋白结合的有毒气体,则B是一氧化碳,B、D的组成元素相同,D为二氧化碳;A可以转化成一氧化碳、二氧化碳,则A为木炭;反应①是工业用赤铁矿炼铁的主要反应,C为赤铁矿的主要成分氧化铁;一氧化碳和氧化铁在高温条件下反应生成铁和二氧化碳,E为铁;F为红色固体单质,可由铁转化而成,说明F是铜,G为黄色溶液,G是含有铁离子的盐溶液。
为单质,B是易与血红蛋白结合的有毒气体,则B是一氧化碳,B、D的组成元素相同,D为二氧化碳;A可以转化成一氧化碳、二氧化碳,则A为木炭;反应①是工业用赤铁矿炼铁的主要反应,C为赤铁矿的主要成分氧化铁;一氧化碳和氧化铁在高温条件下反应生成铁和二氧化碳,E为铁;F为红色固体单质,可由铁转化而成,说明F是铜,G为黄色溶液,G是含有铁离子的盐溶液。
(1)由上分析可知物质D的化学式:CO2;
(2)反应②可以是硫酸铜和铁反应生成硫酸亚铁和铜,反应的现象是:铁的表面有红色固体生成,溶液由蓝色变成浅绿色;
(3)反应③可以是氧化铁和盐酸(或硫酸)反应,化学方程式Fe2O3+6HCl = 2FeCl3+3H2O或Fe2O3+3H2SO4= Fe 2(SO4)3+3H2O。

【题目】据调查,目前市场有一种产品叫“鱼浮灵”,放在鱼缸中可使水中的含氧量增加,某校科学小组的成员对“鱼浮灵”成分进行探究.
(提出问题)“鱼浮灵”的主要成分是什么?
(查阅资料)过碳酸钠,白色结晶颗粒,会与水发生反应,生成碳酸钠和过氧化氢。
(猜想假设)“鱼浮灵”的主要成分是过碳酸钠。
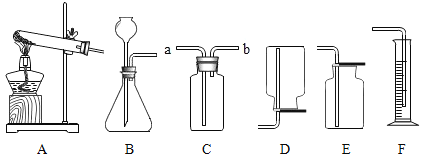
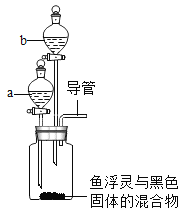
(设计方案)科学小组的成员经过讨论,设计了如图装置,进行探究。
实验 | 主要操作步骤 | 主要实验现象 |
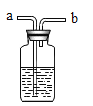
① | 在集气瓶中加入少量“鱼浮灵”与化学式为______的黑色固体, 在仪器 a 中加入新配制的“鱼浮灵”的饱和水溶液;打开仪器 a 的活塞,放出适量溶液后,在导管口放一根带火星的木条 | 木条复燃 |
② | 关闭仪器 a,在仪器 b 中加入______,打开仪器 b 活塞,放出 适量溶液后,在导管口放一燃着的木条。 | 生成大量无色气泡, 木条熄灭 |
(得出结论)“鱼浮灵”的主要成分是过碳酸钠。
根据化学反应方程式:X+H2O═NaCO3+H2O2,推出过碳酸钠的化学式 X 为______。
(实验反思)
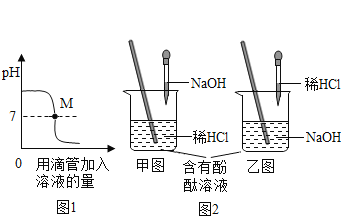
①鱼缸的水中加入“鱼浮灵”,液体的 PH__7。(填“>”、“<”、“=”)
②同学们靖哥哥思考,一致认为实验②不严密,应该补充实验______。
③请写出过碳酸钠与盐酸反应的化学方程式______。
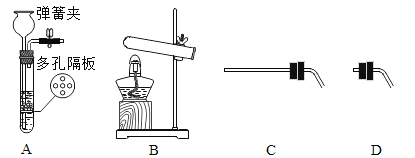
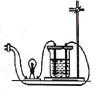
【题目】化学兴趣小组在解老师的带领下探究“饱和氢氧化钙溶液导电性"实验时(如图),发现了一个意外现象:两根石墨电极两端产生氢气、氧气以外,饱和澄清石灰水中出现了白色浑浊。为此,小组同学展开了如下探究。
[提出问题]为什么出现白色浑浊?
[猜想与假设]
甲:可能是饱和溶液电解时________减少,氢氧化钙固体析出导致的浑浊;
乙:可能是饱和溶液通电时温度升高,氢氧化钙固体析出导致的浑浊;
丙:可能是电解过程中产生的___________与饱和石灰水反应导致的浑浊。
[进行实验]小组同学分别设计了如下实验方案验证。
实验步骤 | 实验现象 | 实验结论 | |
甲 | 将90mL相同浓度的饱和澄清石灰水中加入10mL蒸馏水,在相同的电压下再次进行电解实验,观察现象 | _______________。 | 甲同学猜想不正确 |
乙 | 取_____________于烧杯中,加热至电解实验中上升的相同温度,观察现象 | 溶液不变浑浊 | 乙同学猜想____。 |
丙 | 向电解得到浑浊液体中加入足量的稀盐酸,观察现象 | 浑浊消失,有气泡产生。该反应化学方程式为____________。 | 丙同学猜想正确 |
[拓展延伸][注意:若答对以下问题可奖励4分,化学试卷总分不超过60]
为进一步研究丙同学实验后废液成分性质,丁同学取一定质量的废液,逐滴加入溶质质量分数为10.6%的Na2CO3溶液,实验过程中加入Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示:
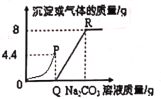
①P点时的溶液中的溶质是____________________(写名称);
②R点对应横坐标的数值为______________________;
③Q至R段表示_________________________________的过程。