��Ŀ����
����Ŀ��(1)ij�о���ѧϰС��Ϊ��֤��������ԭ����ͭ����ʵ�飬����������ϲ�������������
�ʿ�����
I.������һ����ɫ���д̼�����ζ�����壬�ܶȱȿ���С����������ˮ����Һ�ʼ��ԡ�
II.������ԭ����ͭ�Ļ�ѧ��Ӧԭ��2NH3+3CuO![]() 3Cu+N2+3H2O
3Cu+N2+3H2O
ʵ������
��ش�
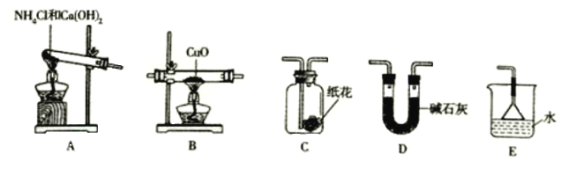
��Ϊ��ɡ�������ԭ����ͭ����ʵ��Ŀ�ģ�װ��A��B��D��E����ȷ����˳��________(�����)��
��װ��A�з�����Ӧ�Ļ�ѧ����ʽ_____________��
��װ��B�۲쵽������________��װ��E������_____________��
��װ��A����������ͨ��װ��C�У�ʯ����Һ���ݵ�ֽ�����ɫ��ԭ����________��
(2)С��ͬѧ�����Ȼ������������������Լ����������ơ�����þ���Ȼ�þ��ƿδ����ǩ����ɫ��Һ�м��������þ��Һ����Ʋ���������ʵ�顣���㲹��ʵ�����ݣ�
ʵ�鲽�� | ʵ������ | ʵ����� |
1.ȡ��֧�־��Թܣ��ֱ���������ɫ��Һ��Ȼ��μ�_________�����۲����� | ______________ | ______________ |
2. ______________ | ______________ | ______________ |
���𰸡�A��C��D��B��E�� (2).�� (3).�� (4).�� (5). (6). (7). (8). (9). (10). (11). Ca��OH��2+2NH4Cl=CaCl2+2H2O+2NH3����ɫ����ͭ��ɺ�ɫ���հ�������ֹ��Ⱦ��������������������ˮ�γɰ�ˮ�Լ�������ʹ��ɫʯ������ɫ�Ȼ�����Һ��֧�Թ������ɰ�ɫ������һ֧�Թ���û����������û��������������Ȼ�þȡ��֧�Թܣ��ֱ������ɰ�ɫ������������Һ���μ�����������Һ�����۲�����һ֧���ְ�ɫ��ɫ������һ֧û�����������а�ɫ������������þ��û������������������
��������
��1�����Ⱦ���Aװ����ȡ������������Cװ�ü��鰱��������Dװ�ó�ȥˮ�֣��پ���Bװ�û�ԭ����ͭ�������Eװ�ó�ȥ��������˳��Ϊ. A��C��D��B��E��
��װ��A�����Ȼ�����������Ʒ�Ӧ�����Ȼ��ơ�������ˮ����Ӧ����ʽΪCa��OH��2+2NH4Cl=CaCl2+2H2O+2NH3����
��װ��B�е������Ǻ�ɫ����ͭ��ɺ�ɫ��װ��E�����������հ�������ֹ��Ⱦ������
��ʯ�������ԭ���ǰ�������ˮ���γɰ�ˮ����ˮ��ʹ��ɫʯ������ɫ��
��2����������Һ�м����Ȼ�����������ǵ����Ȼ�þ������ǵ�������þ�������ƣ���������һ����Һ������ǣ�������Һ����ǣ������Dz�����ǵ����Ȼ�þ��ȡ�����������ƺ�����þ����������������Һ������ǵ�������þ��������ǵ������ƣ�

 ��У����ϵ�д�
��У����ϵ�д�