题目内容
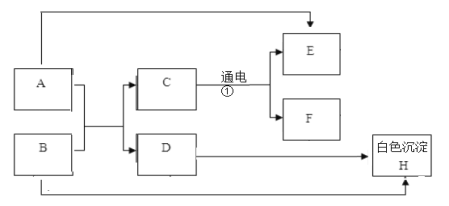
【题目】已知粗盐中含有泥沙、氯化钙和硫酸镁等杂质。为制得纯净的氯化钠固体,某化学兴趣小组进行了如下操作:
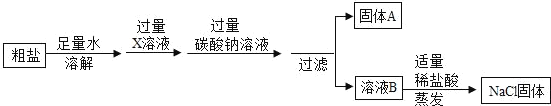
(1)写出用X溶液除杂质的化学方程式。
(2)请设计实验证明溶液B中含有NaOH.(简要写出实验步骤和现象)
(3)工业上可用电解饱和氯化钠溶液的方法制火碱,试写出电解氯化钠溶液的化学方程式。
【答案】Ba(OH)2+MgSO4═Mg(OH)2↓+BaSO4↓ 取少量溶液B于试管中,加入过量的CaCl2溶液,静置,过滤,取上层清液滴加酚酞溶液,溶液变红 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
【解析】
(1)镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氢氧化钡溶液可以将镁离子和硫酸根离子沉淀;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氢氧化钡溶液之后,这样碳酸钠会除去反应剩余的氢氧化钡;X溶液是氢氧化钡溶液,氢氧化钡溶液与硫酸镁溶液反应生成氢氧化镁沉淀和硫酸钡沉淀,反应的化学方程式为:Ba(OH)2+MgSO4═Mg(OH)2↓+Ba SO4↓;
(2)B为氯化钠、氢氧化钠和碳酸钠的混合溶液,碳酸钠溶液呈碱性,对氢氧化钠的检验有干扰,可先用中性的氯化钙溶液将碳酸钠除去,再检验氢氧化钠。实验证明溶液B中含有NaOH方法是取少量溶液B于试管中,加入过量的CaCl2溶液,静置,过滤,取上层清液滴加酚酞溶液,溶液变红;
(3)工业上可用电解饱和氯化钠溶液的方法制火碱,同时生成氢气和氯气,反应的化学方程式为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。

练习册系列答案
相关题目