题目内容
【题目】金属材料在我国建设中起着重要的作用。
(1)铜可以做导线,主要利用了金属铜的延展性和_____;
(2)回收利用是保护金属资源的一条有效途径。某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,已知:Fe+Fe2(SO4)3=3FeSO4。
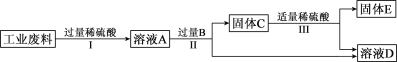
①A~E中含铁元素的有_____(填序号)。
②过程III的反应除溶液颜色变化外,还能观察到_____;
③向AgNO3和Fe(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,滤液为浅绿色。则滤液中一定含有_____(填化学式);
【答案】导电性 ABCD 产生气泡 Zn(NO3)2、Fe(NO3)2
【解析】
(1)铜具有良好的延展性和导电性,所以铜可以做导线,故填导电性。
(2)①工业废料中的氧化铜与氧化铁分别与稀硫酸反应生成硫酸铜、硫酸铁和水,则溶液A中含有铁元素,溶液A中的硫酸铜与B(铁)反应生成硫酸亚铁和铜,硫酸铁与铁反应生成硫酸亚铁,则溶液D中的溶质为硫酸亚铁,含有铁元素,固体C为铜与过量铁的混合物,固体C中的铁与稀硫酸反应生成硫酸亚铁和氢气,固体E为铜,所以含有铁元素的物质有ABCD,故填ABCD。
②过程III的反应是铁与稀硫酸反应生成硫酸亚铁和氢气,观察到的现象是产生气泡,溶液逐渐由无色变为浅绿色,故填产生气泡。
③向AgNO3和Fe(NO3)2的混合溶液中加入一定量的锌粉,锌粉先与硝酸银反应生成银与硝酸锌,硝酸银反应完锌再和硝酸亚铁反应,充分反应后过滤,滤液为浅绿色,则溶液中硝酸亚铁有剩余,锌粉完全反应,所以溶液中的溶质一定有硝酸锌和硝酸亚铁,其化学式分别为Zn(NO3)2、Fe(NO3)2,故填Zn(NO3)2、Fe(NO3)2。

【题目】微观构成是我们学习化学的一个重要组成。甲、乙、丙、丁四种物质,其化学式和微观构成微粒示意图分别列于下表:
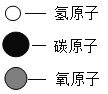
物质 | 甲 | 乙 | 丙 | 丁 | 图例:
|
化学式 | CH4 | C | ? | H2 | |
围观示意图 |
|
|
|
|
(1)甲在高温条件下会生成乙和丁,请写出相应的符号表达式_____。
(2)能保持丁物质化学性质的微粒名称是_____。
(3)元素以游离态在的物质是_____(填“甲、乙、丙、丁”)。
(4)某物质中经查只有H、O两种元素组成,则该物质_____(一定/不一定)是纯净物。