题目内容
【题目】下列四个图象,分别对应四种操作过程,其中正确的是( )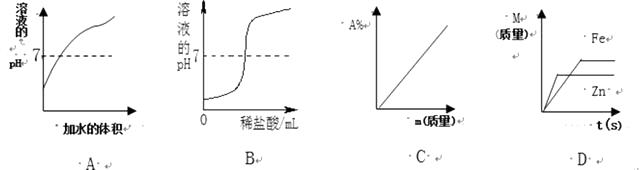
A.向pH=2的酸溶液中不断加水
B.向NaOH溶液中逐滴加入稀盐酸
C.向一定量的水中持续加入食盐(m表示食盐的质量,A%表示溶质质量分数)
D.等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量随反应时间t的变化
【答案】D
【解析】解:A、溶液的pH不会超过7,A错误;
B、向NaOH溶液中逐滴加入稀盐酸,起始溶液为NaOH溶液,显碱性,0点时pH应大于7,,反应结束后为酸溶液,pH应小于7,B错误;
C、当溶液达到饱和后,A%将不再变化,不会一直增加,C错误;
D、锌的活动性比铁强,反应速率比铁快,等质量的锌消耗的稀硫酸比等质量的铁消耗的少,则生成的气体也少,D正确;
故选D。
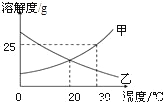
【考点精析】关于本题考查的固体溶解度的影响因素和金属材料的选择依据,需要了解影响固体溶解度的因素:①溶质、溶剂的性质(种类) ②温度:大多数固体物的溶解度随温度升高而升高;如KNO3;少数固体物质的溶解度受温度的影响很小;如NaCl;极少数物质溶解度随温度升高而降低.如Ca(OH)2;黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属才能得出正确答案.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目