题目内容
为测定某铁粉样品(含少量木炭粉)中铁的含量,往盛有219g稀盐酸的烧杯中不断加入铁粉样品,测得生成氢气质量与所加铁粉样品质量的关系如图的所示。
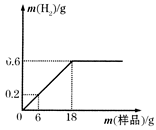
(1)稀盐酸恰好完全反应时,生成氢气的质量为 g。
(2)6g铁粉样品中含铁单质的质量为 g。
(3)求稀盐酸中溶质的质量分数(写出计算过程)。

(1)稀盐酸恰好完全反应时,生成氢气的质量为 g。
(2)6g铁粉样品中含铁单质的质量为 g。
(3)求稀盐酸中溶质的质量分数(写出计算过程)。
(1)0.6 (2)5.6 (3)10%
试题分析:此题是图象型的数据处理题,解答这种题目,要抓住“三点一走势”,即反应刚开始的起始点,反应过程中的横、纵坐标表示的量的走势,反应过程中的转折点,以及反应结束时的终点,,所以根据该题中的图象,不难看出反应结束后产生的氢气质量为0.6g,当加入6g铁粉样品时,产生的氢气质量为0.2g,根据化学方程式中氢气与铁的质量关系是2:56,所以6g铁粉样品中含铁单质的质量为5.6g,再根据化学方程式:Fe + 2HCl=FeCl2 + H2↑中氢气与氯化氢的质量关系,算出稀盐酸中溶质氯化氢的质量,进而求出稀盐酸中溶质的质量分数
解:设铁的质量为x,氯化氢的质量为y
Fe + 2HCl= FeCl2 + H2↑
73 2
y 0.6g
73:2 = y:0.6g
y=21.9g
∴稀盐酸中溶质的质量分数=21.9g/219g×100%=10%

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
 CaO+ CO2↑
CaO+ CO2↑