题目内容
【题目】在老师的指导下,同学们进行了有趣的化学实验探究:
一、测定空气中氧气含量
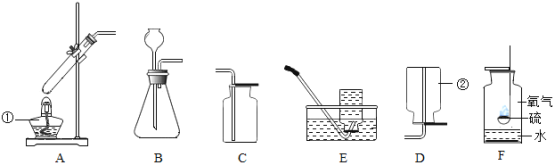
图1所示的是小亮同学用红磷在空气中燃烧的测定方法.过程是:
第1步:将集气瓶容积划分为五等份,并做好标记.
第2步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.
第3步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5.请回答下列问题:
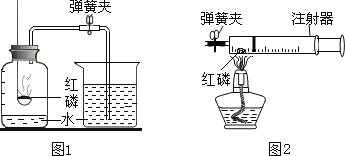
①第2步红磷燃烧时的现象_______________,化学反应表达式____________
②实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是_________.
A、集气瓶底部的水占了一部分体积
B、红磷过少
C、红磷没有燃烧完就急着打开了止水夹
③小博同学对实验进行反思后,提出了改进方法(如图2所示),小博在正式开始实验前,夹紧弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处.该操作的主要目的是_________,你认为改进后的优点是_________
二、小余阅读课外资料得知:双氧水分解除了用二氧化锰(MnO2)还可用氧化铜(CuO)等物质作催化剂,于是他对氧化铜产生了探究兴趣.
(提出问题)氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
(设计实验)小余以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)
实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
① | 1.2g | / | |
② | 1.2g | CuO 0.5g | |
③ | 1.2g | MnO20.5g |
①上述实验应测 量的“待测数据”是时间__________.
②若实验②比实验①的“待测数据”_________(填“大”或“小”),说明氧化铜能加快氯酸钾的分解.
③将实验②反应剩余的固体取出后经洗涤、干燥,再次精确称量得到0.5g黑色粉末,这样做的目的是________,小余同学认为氧化铜肯定是氯酸钾分解的催化剂,但小淳同学对此提出了异议,小淳同学设计了如下实验:将第二次精确称量得到的0.5g黑色粉末和1.2g氯酸钾混合放入试管中,加热,伸入带火星木条,发现木条很快复燃.小淳同学这样做目的是________,
(预期结论)氧化铜也能作氯酸钾的催化剂.
(评价设计)你认为小余设计实验③和实验②对比的目的是__________; 写出实验②反应的表达式______
【答案】发黄光、放出热量、冒出大量的白烟 ![]() BC 检查装置气密性 没有白烟进入空气,环保 时间 小 验证氧化铜质量不变 验证氧化铜化学性质不变 比较氧化铜和二氧化锰的催化效果
BC 检查装置气密性 没有白烟进入空气,环保 时间 小 验证氧化铜质量不变 验证氧化铜化学性质不变 比较氧化铜和二氧化锰的催化效果 ![]()
【解析】
一、红磷在空气中燃烧的现象:发黄光、放出热量、冒出大量的白烟;要使本实验成功,必须注意以下几点:装置的气密性好;白磷足量;必须冷却到室温再读数;小博操作的主要目的是检验装置气密性;改进后的优点是:没有白烟进入空气,环保或不会有空气溢出,测量精确或直接读数,测量精确;故答案为:①发黄光、放出热量、冒出大量的白烟;![]() ;②BC;③检验装置气密性;没有白烟进入空气,环保(不会有空气溢出,测量精确或直接读数,测量精确)
;②BC;③检验装置气密性;没有白烟进入空气,环保(不会有空气溢出,测量精确或直接读数,测量精确)
二、由实验数据可知:上述实验应测量的“待测数据”是:时间或收集一定体积氧气所需时间;若实验②比实验①的“待测数据”更小,说明氧化铜能加快氯酸钾的分解;将实验②反应剩余的固体取出后经洗涤、干燥,再次精确称量得到0.5g黑色粉末,这样做的目的是验证氧化铜质量不变;小淳同学这样做目的是:验证氧化铜化学性质不变;小余设计实验③和实验②对比的目的是:比较氧化铜和二氧化锰的催化效果;氯酸钾在氧化铜做催化剂和加热的条件下生成氯化钾和氧气;故答案为:①时间(收集一定体积氧气所需时间);②小;③验证氧化铜质量不变;验证氧化铜化学性质不变;比较氧化铜和二氧化锰的催化效果;![]()

【题目】已知化学反应X+Y=Z,现进行了两次实验,测得数据如表所示:
实验序号 | 反应物的质量/g | 产物Z的质量/g | |
X | Y | ||
① | 9.0 | 1.6 | 9.6 |
② | 5.0 | 2.4 | 6.0 |
若将①和②的反应物全部混合在一起,最多可生成产物Z( )
A. 16.6g B. 16.8g C. 17.0g D. 15.6g
【题目】某化学兴趣小组在实验室用氯酸钾和二氧化锰混合加热制取氧气时,发现制得的气体有刺激性气味,于是在老师的指导下对该气体成分进行探究。
(提出问题) 氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
(查阅资料)
①氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
②氯气(Cl2)是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
(1)(猜想与假设)
猜想一:该气体为O2;猜想二:该气体为Cl2;猜想三:该气体为________。
(2)(实验探究)
序号 | 实验操作 | 实验现象 | 实验结论 |
① | 小丽用排水集气法收集A、B两瓶气体,将带火星木条伸入A中;湿润的淀粉碘化钾试纸伸入B中 | A中带火星木条复燃,B中淀粉碘化钾试纸不变色 | 猜想___成立 |
② | 小岚用向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,湿润的淀粉碘化钾试纸伸入D中 | C中带火星木条复燃,D中淀粉碘化钾试纸_______ | 猜想三成立 |
(3)(反思与评价)①小涛认为小丽的结论不正确,原因是_____。
②还可用蓝色石蕊试纸检验Cl2的存在。
(4)(拓展应用) MnO2不仅能作催化剂还可以作反应物,实验室通常用MnO2与浓盐酸共热制取Cl2,同时生成+2价的锰的氯化物和另一种常见的化合物,请写出该反应的化学方程式:___________。
(5)实验室除了用氯酸钾制取氧气,还可用高锰酸钾或过氧化氢溶液制取氧气,请分别写出实验室用高锰酸钾、过氧化氢溶液制取氧气的化学方程式: ___________、______________;