题目内容
氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源,反应的化学方程式为:LiH + H2O=LiOH + H2↑。据此计算:
(1)(1分)在LiH中,Li元素显+1价,则H元素显 价。
(2)(5分)计算80 g氢化锂与足量的水反应生成氢气的质量
(1)(1分) -1
(2)(5分)
解:设生成氢气的质量为x
LiH + H2O=LiOH + H2↑ ………………………………(1分)
8 2
80g x ………………………………(1分)
 ………………………………(1分)
………………………………(1分)
解得x=20g ………………………………(2分)
答:生成氢气的质量为20g

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
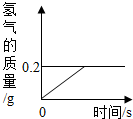 (2013?安庆二模)氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与水反应,得到100g氢氧化锂(LiOH)溶液,同时产生了氢气(LiH+H2O=LiOH+H2↑).产生氢气的质量与反应时间的关系如图所示,则所得氢氧化锂溶液的质量分数为多少?
(2013?安庆二模)氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与水反应,得到100g氢氧化锂(LiOH)溶液,同时产生了氢气(LiH+H2O=LiOH+H2↑).产生氢气的质量与反应时间的关系如图所示,则所得氢氧化锂溶液的质量分数为多少?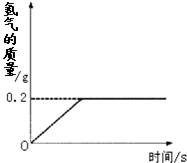 氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与99.4克水反应,产生气体的质量与反应时间的关系如图所示,请回答下列问题:
氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与99.4克水反应,产生气体的质量与反应时间的关系如图所示,请回答下列问题: LiOH + H2↑。计算80 g氢化锂与足量的水反应生成氢气的质量。
LiOH + H2↑。计算80 g氢化锂与足量的水反应生成氢气的质量。