题目内容
硝酸铵(NH4NO3)是农业生产中的一种化肥.因为其中含有铵根离子(NH+)和硝酸根离子(NO3- ),因此称为铵盐,又可称为硝酸盐.试据化学式回答:
(1)硝酸铵中氮元素的化合价是不同的,其中氮元素高价是 ;
(2)硝酸铵硝酸铵相对分子质量是,其中氮、氢、氧各元素的质量比为 .
(1)硝酸铵中氮元素的化合价是不同的,其中氮元素高价是
(2)硝酸铵硝酸铵相对分子质量是,其中氮、氢、氧各元素的质量比为
考点:有关元素化合价的计算,元素质量比的计算
专题:化学式的计算
分析:(1)根据硝酸铵的化学式为NH4NO3,利用物质的类别和原子团的化合价来进行计算.
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答.
根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答.
根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答:解:(1)因硝酸铵是盐类化合物,是由阴阳离子构成的,铵根离子带1个单位的正电荷,硝酸根离子带1个单位的负电荷,则铵根的化合价为+1价,硝酸根的化合价为-1价,在铵根中,H元素的化合价为+1价,设N元素的化合价为x,则
x+(+1)×4=+1
解得x=-3,即铵根中氮元素的化合价为-3价;
在硝酸根中,氧元素的化合价为-2价,设N元素的化合价为y,则
y+(-2)×3=-1
解得y=+5,即硝酸根中氮元素的化合价为+5价;
故填:+5.
(2)NH4NO3的相对分子质量为14×2+1×4+16×3=80;硝酸铵中氮、氢、氧三种元素的质量之比是(14×2):(1×4):(16×3)=7:1:12.
故填:80;7:1:12.
x+(+1)×4=+1
解得x=-3,即铵根中氮元素的化合价为-3价;
在硝酸根中,氧元素的化合价为-2价,设N元素的化合价为y,则
y+(-2)×3=-1
解得y=+5,即硝酸根中氮元素的化合价为+5价;
故填:+5.
(2)NH4NO3的相对分子质量为14×2+1×4+16×3=80;硝酸铵中氮、氢、氧三种元素的质量之比是(14×2):(1×4):(16×3)=7:1:12.
故填:80;7:1:12.
点评:本题考查元素化合价的计算,比较复杂,学生解答的难点是往往将N元素的化合价理解为一种,利用化合物中正负化合价的代数和为0来直接计算,而错答,学生应熟悉常见原子团的化合价.

练习册系列答案
相关题目
下列关于氧气的说法正确的是( )
| A、氧气易溶于水 |
| B、氧气有可燃性 |
| C、氧气可以支持燃烧 |
| D、空气中氧气含量最大 |
如图是三种微粒的结构示意图,有关它们的说法正确的是( )
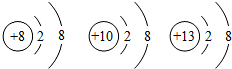
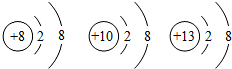
| A、它们的原子核外电子层数相同 |
| B、它们的化学性质相同 |
| C、它们属于同种元素的粒子 |
| D、它们都是原子 |