题目内容
化学式为AB2的化合物,式量为46.其中A的百分含量为30.4%,则B的原子量为( )
【答案】分析:根据物质中某元素的质量分数= ×100%,和相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答.
×100%,和相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答.
解答:解:A的百分含量为30.4%,则有:30.4%=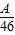 ×100%,则A的相对原子质量为:46×30.4%=14;
×100%,则A的相对原子质量为:46×30.4%=14;
B的原子量为:(46-14)÷2=16;
故选B.
点评:本题考查学生根据物质中某元素的质量分数进行分析解题的能力.
 ×100%,和相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答.
×100%,和相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答.解答:解:A的百分含量为30.4%,则有:30.4%=
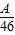 ×100%,则A的相对原子质量为:46×30.4%=14;
×100%,则A的相对原子质量为:46×30.4%=14;B的原子量为:(46-14)÷2=16;
故选B.
点评:本题考查学生根据物质中某元素的质量分数进行分析解题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(1)下表列出了部分人体中含量较多元素的原子结构示意图.请据表回答下列问题:
| H | O | Na | Mg | Cl | K | Ca |
 |  |  |  |  |  |  |
②K+的核外电子数为________; 与氧元素形成化合物的化学式为________.
③金属钠、钾的化学性质有许多相似之处,其原因是________.
④上表中的元素两两化合,能形成AB2型化合物的化学式为________(写一种).
(1)下表列出了部分人体中含量较多元素的原子结构示意图.请据表回答下列问题:
①属于第二周期的元素是______.
②K+的核外电子数为______;
③金属钠、钾的化学性质有许多相似之处,其原因是______.
④上表中的元素两两化合,能形成AB2型化合物的化学式为______(写一种).
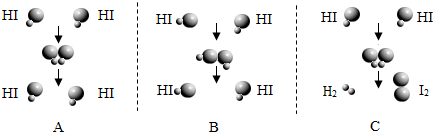
(2)在化学反应中,反应物分子间相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起化学反应.下图表示HI(碘化氢)分子之间的几种碰撞示意图,有些HI分子碰撞后,会发生化学反应产生H2和I2,有些碰撞不会发生反应.图中大球表示碘原子,小球表示氢原子.

①A、B、C三图中,表示HI分子碰撞后发生了化学反应的是______图(选填序号).
②请写出上述所发生反应的化学方程式:______.
③若要得到1个H2分子,至少需要______个HI分子碰撞.
| H | O | Na | Mg | Cl | K | Ca |
 |  |  |  |  |  |  |
②K+的核外电子数为______;
③金属钠、钾的化学性质有许多相似之处,其原因是______.
④上表中的元素两两化合,能形成AB2型化合物的化学式为______(写一种).
(2)在化学反应中,反应物分子间相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起化学反应.下图表示HI(碘化氢)分子之间的几种碰撞示意图,有些HI分子碰撞后,会发生化学反应产生H2和I2,有些碰撞不会发生反应.图中大球表示碘原子,小球表示氢原子.

①A、B、C三图中,表示HI分子碰撞后发生了化学反应的是______图(选填序号).
②请写出上述所发生反应的化学方程式:______.
③若要得到1个H2分子,至少需要______个HI分子碰撞.