题目内容
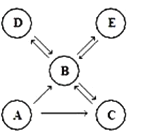
【题目】将一定质量的A、B、C、D四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下表:
物质 | A | B | C | D |
反应前的质量/g | 4 | 10 | 1 | 25 |
反应后的质量/g | 待测 | 21 | 10 | 9 |
若A的相对分子质量为n,D的相对分子质量为2n,则下列说法正确的是( )
A.该反应中生成B与C的质量比为21:10
B.该反应不遵循质量守恒定律
C.该反应中A与D的化学计量数之比为1:2
D.该反应是分解反应
【答案】C
【解析】
根据表格数据,分别对比A、B、C、D四种物质在密闭容器中的前后质量增或减少的量,应用质量守恒定律,进行判断,B、C反应后质量增加,说明它们是生成物,且生成的质量分别为:B的生成质量21-10=11g;C的生成质量10-1=9g。D反应后质量减少,说明是反应物,参加反应的质量25-9=16g,反应物总质量16g小于生成物总质量(11g+9g),所以A为反应物,且参加反应的质量11g+9g-16g=4g。因此该反应的各物质的质量关系为:
 。
。
A、根据该反应的各物质的质量关系,反应中生成B与C的质量比为11:9,不符合题意;
B、该反应不遵循质量守恒定律,说法不正确,一切化学反应都遵守质量守恒定律,不符合题意;
C、设反应中反应物A、D的计量数之比为x:y。已知A的相对分子质量为n,D的相对分子质量为2n,则


因此,反应中A与D的化学计量数之比为1:2,符合题意;
D、该反应是![]() ,不属于分解反应,不符合题意。故选C。
,不属于分解反应,不符合题意。故选C。

【题目】同学们在学习了焦炭还原氧化铁的反应后,联想到单质碳的一些化学性质,对反应后的气体成份产生了疑问,并对其气体成份进行了如下探究。
(猜想)①气体产物全部是CO2;②气体产物全部是_____;③气体产物是CO和CO2的混合物。
(查阅资料)CO气体能使湿润的黄色氯化钯试纸变蓝色。
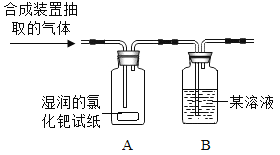
(设计实验)根据各自的猜想,他们共同设计了如下图的实验装置进行探究。
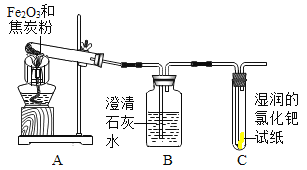
(现象与分析)
预期的现象 | 相应的结论 |
如果装置B中澄清石灰水变浑浊,装置C无明显现象; | 则猜想①成立; |
如果装置B中澄清石灰水变无明显变化,装置C_____; | 则猜想_____成立; |
如果装置B_____,装置C_____; | 则猜想_____成立。 |
(结论)根据实验结果猜想③成立,同学们的疑问是合理的。
(反思)
(1)同学们对CO产生的原因进行了首先Fe2O3与焦炭反应,生成的其中一种产物和焦炭又发生了化学反应,产生了CO;请你写出该化学反应涉及的两个化学方程式:_____、_____。
(2)根据上述实验,可以得出焦炭具有_____性。