题目内容
【题目】请结合下图回答问题:
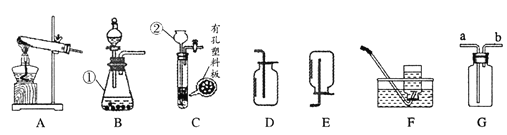
(1)写出图中有标号仪器的名称:①________,②________。
(2)实验室用加热暗紫色固体制取氧气,选用的发生装置是________ (填字母),装置需要改进的地方是________。写出该反应的化学方程式________________________________,实际反应中收集到的氧气质量比理论值多,可能的原因是________。
(3)用B、D装置组合可制取并收集另外一种常见气体,写出制取该气体的化学方程式___;有同学认为用装置C比B更好,理由为_________;检验气体收集满的方法是____。
(4)甲烷是一种无色无味、难溶于水、密度比空气小的气体。实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷时,发生装置应选用________;若用G装置收集气体,则气体应从________导管口通入。
【答案】 锥形瓶 长颈漏斗 A 试管口放一团棉花 2KMnO4=K2MnO4 + MnO2 + O2↑ K2MnO4可能分解放出氧气 CaCO3 + 2HCl == CaCl2 + CO2↑+ H2O 可控制反应的发生和停止 燃着的木条放在瓶口火焰熄灭 A b
【解析】(1)仪器①的名称是锥形瓶,仪器②的名称是长颈漏斗;
(2)加热暗紫色固体制取氧气,是用高锰酸钾制取氧气,该反应的反应物的状态是固体,反应条件是加热,故选固固加热型装置A;高锰酸钾分解的速率很快,易将高锰酸钾粉末带入导管而堵塞导管,故需要在试管口放一团棉花;该反应是高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的方程式为:2KMnO4△ K2MnO4+MnO2+O2↑;实际反应中收集到的氧气质量比理论值多,可能是由于K2MnO4可能分解放出氧气 ;
(3)B装置是固液不加热型装置,可以制取二氧化碳,该反应是用碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,反应方程式为;CaCO3+2HCl == CaCl2+H2O+CO2↑;C装置中需要稀盐酸的量较少,且可控制反应的发生和停止,而B装置加入稀盐酸后直到药品反应完才能停止;具有二氧化碳气体收集满的方法是将燃着的木条放在瓶口,如火焰熄灭则满;
(4) 甲烷的制取的反应物的状态是固体,反应的条件是加热,故选固固加热型装置A;
装置G 是多功能装置,此处改装为排空气法收集甲烷,由于甲烷的密度比空气的密度小,故选向下排空气法收集,故短进长出,从b管导入;

【题目】有关物质组成及化学规律的发现对化学的发展做出了重要贡献。
(1)法国化学家拉瓦锡为化学学科的发展做出了巨大贡献,下列有关发现与他有密切关系的是。
A. 空气的组成 B. 质量守恒定律 C. 水的组成 D. 酸碱指示剂
(2)在密闭容器内加入下列两种物质,并称量加入前后的总质量(含密闭容器),能验证质量守恒定律的是 (填标号)。
A.蔗糖和水
B.氯化钠溶液和硝酸钾溶液
C.氯化钡溶液和稀硫酸
(3)在氧气中点燃红磷的实验过程,固体质量变化如图所示。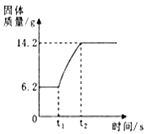
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是。
②该反应的化学方程式为。
③参加反应的氧气质量为g。
(4)某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。
查阅资料可知Mg、Mg3N2能发生如下反应:
①2Mg+O2 ![]() 2MgO; ②3Mg+N2
2MgO; ②3Mg+N2 ![]() Mg3N2; ③2Mg+CO2
Mg3N2; ③2Mg+CO2 ![]() 2MgO+C
2MgO+C
④Mg+H2O ![]() MgO+H2↑ ⑤Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
MgO+H2↑ ⑤Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
实验中所用的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。回答下列问题: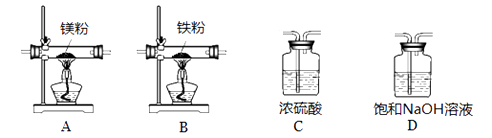
①连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是(填装置序号)。D装置中发生反应的化学方程式为
②通气后,如果同时点燃A、B装置的酒精灯,对实验结果有何影响?。
③设计一个实验,验证产物是否含氮化镁:
实验操作和实验现象 | 实验结论 |
产物中含有氮化镁 |
④思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N的质量,请给出合理的解释。
【题目】合理利用资源和保护环境是我们关注的问题。请回答:
(1)化石燃料是一类重要能源,它包括煤、石油和。
(2)煤作为燃料给我么们带来了益处,但对环境也造成了不良影响。
①下列关于酸雨的叙述正确的是(填序号)
A. 腐蚀大理石雕像 B. 是由二氧化碳和二氧化硫引起的
C. 酸化土壤 D. 对海洋生物没有影响
②使燃料充分燃烧,通常除了考虑燃烧时要有足够的空气,还要考虑;
(3)为减少污染,城市公共交通正大力推广使用压缩天然气或液化石油气为动力。某种清洁燃料的主要成份是A,一定质量的A物质在B物质中充分燃烧,如下表所示)。
物 质 | A | B | C | D |
|
分子示意图 | ? |
|
|
| |
反应前质量/g | 44 | ? | 0 | 0 | |
反应后质量/g | 0 | 0 | 132 | 72 |
①在上述反应中提供氧、具有氧化性的物质为。(写化学式)
②A物质中各元素的质量比为__。