题目内容
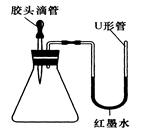
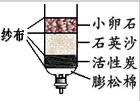
过氧化钠(Na2O2)是一种黄色固体。某次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入右图烧杯中,缓慢倒人CO2后发现处于下位的蜡烛先熄灭,上位的后熄灭,同时又惊奇的发现棉花燃烧起来。
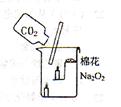
I.实验过程中“下位的蜡烛先熄灭,上位的后熄灭”的现象
说明二氧化碳具有的性质是______________________。
Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了我们已知“棉花是可燃物”之外,还需满足的条件为_________________________________。
【提出问题】在实验中是如何给棉花燃烧提供上述条件的呢?
【查阅资料】2Na2O2+2CO2=Na2CO3+O2↑; 2Na2O2+2H2O=4NaOH+O2↑;
白色的无水硫酸铜遇水会变呈蓝色。

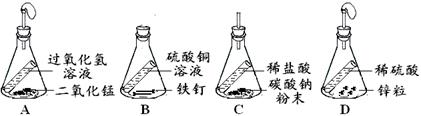
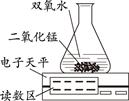
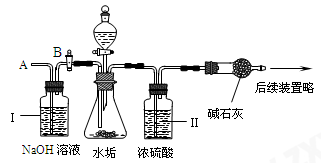
【设计实验】经过讨论后,小组同学设计了如下图的实验进行探究。
【实验步骤】 (1)按上图装配好装置,并检查其气密性;
(2)将相关的试剂放入对应的仪器中;
(3)推动注射器的活塞,把稀盐酸注入锥形瓶内,并固定活塞位置;
A中发生的反应方程式为________________________;
(4)一段时间后,在a处放置一根带火星的小木条,观察现象。
【实验现象】 (1)C中干燥管中没有出现蓝色
(2)a处带火星的小木条复燃;
(3)D处烧杯中水的温度升高。
【实验分析】 (1)B装置的作用是____________;为什么要有此装置__________________;
(2)C装置的作用是_________________;
(3)D装置的烧杯内水温升高的原因是_____________________________。
【实验结论】 “小木条复燃”说明了Na2O2和CO2反应产生了氧气并放出热量;满足了棉花燃烧的条件,棉花的主要成分为纤维素,可用(C6Hl0O5)n来表示,试写出纤维素完全燃烧的方程式___________________________________________________。

I.实验过程中“下位的蜡烛先熄灭,上位的后熄灭”的现象
说明二氧化碳具有的性质是______________________。
Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了我们已知“棉花是可燃物”之外,还需满足的条件为_________________________________。
【提出问题】在实验中是如何给棉花燃烧提供上述条件的呢?
【查阅资料】2Na2O2+2CO2=Na2CO3+O2↑; 2Na2O2+2H2O=4NaOH+O2↑;
白色的无水硫酸铜遇水会变呈蓝色。

【设计实验】经过讨论后,小组同学设计了如下图的实验进行探究。
【实验步骤】 (1)按上图装配好装置,并检查其气密性;
(2)将相关的试剂放入对应的仪器中;
(3)推动注射器的活塞,把稀盐酸注入锥形瓶内,并固定活塞位置;
A中发生的反应方程式为________________________;
(4)一段时间后,在a处放置一根带火星的小木条,观察现象。
【实验现象】 (1)C中干燥管中没有出现蓝色
(2)a处带火星的小木条复燃;
(3)D处烧杯中水的温度升高。
【实验分析】 (1)B装置的作用是____________;为什么要有此装置__________________;
(2)C装置的作用是_________________;
(3)D装置的烧杯内水温升高的原因是_____________________________。
【实验结论】 “小木条复燃”说明了Na2O2和CO2反应产生了氧气并放出热量;满足了棉花燃烧的条件,棉花的主要成分为纤维素,可用(C6Hl0O5)n来表示,试写出纤维素完全燃烧的方程式___________________________________________________。
I.密度比空气的密度大;不能燃烧,也不能支持燃烧
Ⅱ.与氧气(或空气)接触 温度达到着火点
【实验步骤】(3)CaCO3+2HCl=CaCl2+H2O+CO2↑
【实验分析】(1)除去二氧化碳中的水蒸气 防止水与Na2O2反应生成氧气
(2)检验二氧化碳中水蒸气是否除尽
(3)Na2O2和CO2反应放出了热量
【实验结论】 (C6H10O5)n+6nO2点燃5nH2O+6nCO2
Ⅱ.与氧气(或空气)接触 温度达到着火点
【实验步骤】(3)CaCO3+2HCl=CaCl2+H2O+CO2↑
【实验分析】(1)除去二氧化碳中的水蒸气 防止水与Na2O2反应生成氧气
(2)检验二氧化碳中水蒸气是否除尽
(3)Na2O2和CO2反应放出了热量
【实验结论】 (C6H10O5)n+6nO2点燃5nH2O+6nCO2
试题分析:I.实验过程中“下位的蜡烛先熄灭,上位的后熄灭”的现象说明二氧化碳密度比空气的密度大;不能燃烧,也不能支持燃烧。
Ⅱ.棉花燃烧需满足的条件为:与氧气(或空气)接触、温度达到着火点。
【实验步骤】(3)A中是碳酸钙和盐酸反应,反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
【实验分析】 (1)B装置中是浓硫酸,其作用是除去二氧化碳中的水蒸气;此装置的作用是防止水与Na2O2反应生成氧气;
(2)C装置中是无水硫酸铜,其作用是检验二氧化碳中水蒸气是否除尽;
(3)D装置的烧杯内水温升高的原因是Na2O2和CO2反应放出了热量。
【实验结论】纤维素完全燃烧的方程式为(C6H10O5)n+6nO2点燃5nH2O+6nCO2。
点评:二氧化碳密度比空气的密度大,不能燃烧,也不能支持燃烧,可做灭火剂。
燃烧必须同时具备三个条件才可以:1、有可燃物;2、可燃物与氧气接触;3、温度达到可燃物的着火点。
浓硫酸具有吸水性,可做干燥剂;无水硫酸铜遇水变蓝色,可以用来检验水的存在与否。

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目