题目内容
【题目】下表是KNO3 、NaCl在不同温度下的部分溶解度数据,请回答问题:
温度(℃) | 10 | 20 | 40 | 60 | 80 |
KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
① 10℃时,NaCl 溶解度是__________。
② 在20℃时,将50克硝酸钾溶解在100克水中,形成的是__________(填“饱和”或“不饱和”)溶液,若升温至40℃,形成的溶液质量为_________g,则烧杯中溶液的溶质质量分数为__________(精确到0.1%)
③ 某温度时,氯化钠与硝酸钾的溶解度相等,则溶解度的最小取值范围是__________。
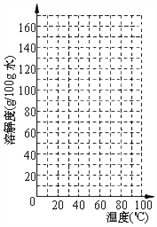
④ 根据表中数据,请在坐标图中描点、绘制符合KNO3溶解度变化规律的曲线__________。
⑤ 固体硝酸钾中混有少量氯化钠可以通过溶解、蒸发浓缩、降温结晶、过滤等步骤分离提纯硝酸钾。可以利用该方法分离的理由是__________。
Ⅰ. 固体混合物中硝酸钾的含量较高,氯化钠的含量较低
Ⅱ. 硝酸钾的溶解度受温度影响变化较大
Ⅲ. 40℃至100℃,硝酸钾的溶解度始终大于氯化钠
⑥ 气体的溶解度也有一定的变化规律。不同温度下,氧气的溶解度随压强变化如右图所示,图中t2对应的温度为30℃,则t1对应的温度_________。
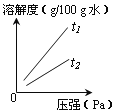
A.小于30℃ B.等于30℃ C.大于30℃ D.无法确定
【答案】35.8g/100g水饱和15033.3%36 g/100g水 <S<36.6 g/100g水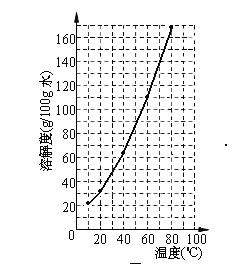 (评分要求:能清楚看到五个描点;光滑的曲线)Ⅰ ⅡA
(评分要求:能清楚看到五个描点;光滑的曲线)Ⅰ ⅡA
【解析】由表格数据可知,10℃时,NaCl 溶解度是35.8g;(2)20℃时,硝酸钾的溶解度是31.6g,即该温度下,100g水中最多溶解31.6g硝酸钾形成饱和溶液,现将50克硝酸钾溶解在100克水中,硝酸钾不能完全溶解,形成的是饱和溶液;40℃时,硝酸钾的溶解度为63.9g,硝酸钾完全溶解,故形成的硝酸钾的不饱和溶液,溶液的质量=100g+50g=150g;溶质的质量分数=![]() =33.3%;(3)由KNO3 、NaCl的溶解度数据可知,在20℃-40℃的某一温度时,氯化钠与硝酸钾的溶解度相等,溶解度的范围是36g-36.6g;(4)找到对应温度下物质的溶解度,然后用光滑的曲线将这些点连接起来;(5)由于硝酸钾的溶解度随温度的变化变化较大,故硝酸钾中含有少量的氯化钠时可用降温结晶的方法提纯硝酸钾,故选Ⅰ、Ⅱ;(6)气体的溶解度随温度的升高而减小,随压强的增大而增大,故选A。
=33.3%;(3)由KNO3 、NaCl的溶解度数据可知,在20℃-40℃的某一温度时,氯化钠与硝酸钾的溶解度相等,溶解度的范围是36g-36.6g;(4)找到对应温度下物质的溶解度,然后用光滑的曲线将这些点连接起来;(5)由于硝酸钾的溶解度随温度的变化变化较大,故硝酸钾中含有少量的氯化钠时可用降温结晶的方法提纯硝酸钾,故选Ⅰ、Ⅱ;(6)气体的溶解度随温度的升高而减小,随压强的增大而增大,故选A。