题目内容
【题目】关于溶液的说法错误的是
A. 固体、液体、气体都可以做溶质
B. 溶液一定是均一、稳定的混合物
C. 欲使100克KNO3溶液的质量分数由5%变成10%,可向其中加入5克KNO3固体
D. 25℃时,将KNO3溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量不一定相等
【答案】C
【解析】均一、稳定的混合物都是溶液,溶液一定是混合物。所以溶液、溶质、溶剂都可能为固体、液体、气体;![]() ,欲使100克KNO3溶液的质量分数由5%变成10%,可向其中加入50/9克KNO3固体;
,欲使100克KNO3溶液的质量分数由5%变成10%,可向其中加入50/9克KNO3固体;
25℃时,将KNO3溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,b ≥a。如果开始时的硝酸钾溶液是饱和的,二者相等,开始溶液不饱和,b>a。故选C

【题目】下表是KNO3 、NaCl在不同温度下的部分溶解度数据,请回答问题:
温度(℃) | 10 | 20 | 40 | 60 | 80 |
KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
① 10℃时,NaCl 溶解度是__________。
② 在20℃时,将50克硝酸钾溶解在100克水中,形成的是__________(填“饱和”或“不饱和”)溶液,若升温至40℃,形成的溶液质量为_________g,则烧杯中溶液的溶质质量分数为__________(精确到0.1%)
③ 某温度时,氯化钠与硝酸钾的溶解度相等,则溶解度的最小取值范围是__________。
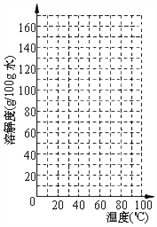
④ 根据表中数据,请在坐标图中描点、绘制符合KNO3溶解度变化规律的曲线__________。
⑤ 固体硝酸钾中混有少量氯化钠可以通过溶解、蒸发浓缩、降温结晶、过滤等步骤分离提纯硝酸钾。可以利用该方法分离的理由是__________。
Ⅰ. 固体混合物中硝酸钾的含量较高,氯化钠的含量较低
Ⅱ. 硝酸钾的溶解度受温度影响变化较大
Ⅲ. 40℃至100℃,硝酸钾的溶解度始终大于氯化钠
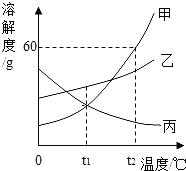
⑥ 气体的溶解度也有一定的变化规律。不同温度下,氧气的溶解度随压强变化如右图所示,图中t2对应的温度为30℃,则t1对应的温度_________。
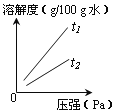
A.小于30℃ B.等于30℃ C.大于30℃ D.无法确定