题目内容
【题目】根据下图甲、乙、丙三种固体(均不含结晶水)的溶解度曲线回答:
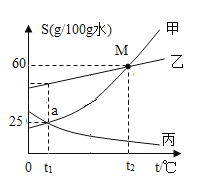
(1)t1℃甲物质的溶解度是_____。
(2)t2℃时,对 50g 甲物质投入到 80g 水中充分溶解,溶质与溶液的质量比为_____。
(3)t1℃时,对恰好处于 a 点状态的甲的溶液,升温至 t2℃,溶质质量分数_____(选填“变大”、“变小”或“不变”)。
(4)分别将 t2℃的三种物质的饱和溶液 100g 降温到 t1℃时,甲、乙、丙溶液质量由大到小关系为_____(选 填“<”、“>”或“=”)。
(5)溶液甲中含有少量的乙,提纯甲物质的方法是_____。
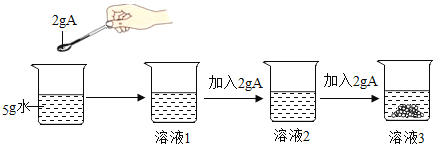
(6)A 是 t2℃含有 120g 水的甲物质的溶液,经过如下操作,得到 32g 甲的固体。
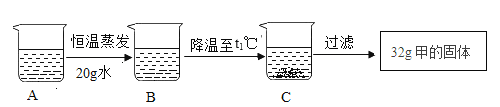
Ⅰ. A 溶液为_____(选填“饱和”或“不饱和”)溶液。
关于溶质的质量分数:溶液 B_____溶液 C(选填“>”、“>”或“=”)。
Ⅱ. 对 A→C 的过程的分析,正确的是_____(选填编号)。
a A 到 B 的过程中,溶质质量不变
b B 中溶质与溶剂的质量比为 57:100
c A 中溶液的质量等于 187g
d 无法比较A、C 烧杯中溶液溶质的质量分数
(7)欲配制 200g 溶质质量分数为 5%的丙物质的溶液,需要固体丙_____g,水_____mL。
【答案】25g/100g水 3:8 不变 丙>乙>甲 降温结晶 不饱和 > ab 10 190
【解析】
(1)由图可知,t1℃甲物质的溶解度是25g/100g水。
(2)由图可知,t2℃时,甲物质的溶解度是60g/100g水。对 50g 甲物质投入到 80g 水中充分溶解,所溶解的甲物质的质量为48g。故溶质与溶液的质量比为48g:(48+80)g=3:8。
(3)t1℃时,对恰好处于 a 点状态的甲的溶液,升温至 t2℃,溶质、溶剂的质量均不变,故溶质质量分数不变。
(4)甲、乙的溶解度随温度的升高而降低,且甲的溶解度大于乙的溶解度,丙的溶解度随温度的升高而降低。升高温度甲析出的质量大于乙的质量,丙无晶体析出。故分别将 t2℃的三种物质的饱和溶液 100g 降温到 t1℃时,甲、乙、丙溶液质量由大到小关系为:丙>乙>甲。
(5)甲、乙的溶解度随温度的升高而增大,且甲的溶解度受温度的影响较大,故溶液甲中含有少量的乙,提纯甲物质的方法是:降温结晶。
(6)Ⅰ. A 溶液恒温蒸发20g水后得到B溶液,且B溶液中无晶体,B降温至t1℃后,得到C,C中有未溶解的晶体,故A 、B溶液均为不饱和溶液。
关于溶质的质量分数:B、C中溶剂质量相等,C中有未溶解的晶体,故溶液 B中溶质质量分数>溶液 C中溶质质量分数。
Ⅱ. a、A 到 B 的过程是恒温蒸发水,且A 、B溶液均为不饱和溶液,故该过程中,溶质质量不变,正确;
b、C是t1℃时的饱和溶液,且此时溶剂的质量为100g,故C中溶质的质量为25g。C过滤后得到得到 32g 甲的固体,故B中溶质的质量为25g+32g=57g。因此B 中溶质与溶剂的质量比为 57:100,正确;
c、A 中溶液的质量=120g+57g=177g,错误;
d、A 烧杯中溶液溶质的质量分数=![]() ×100%≈32.2%>C烧杯中溶液溶质的质量分数=
×100%≈32.2%>C烧杯中溶液溶质的质量分数=![]() ×100%=20%,错误。故选ab;
×100%=20%,错误。故选ab;
(7)欲配制 200g 溶质质量分数为 5%的丙物质的溶液,需要固体丙200g×5%=10g,需要水的质量为200g-10g=190g,约190mL。