题目内容
【题目】钠及化合物是中学化学元素学习和研究的重要内容。
(1)下图是钠的原子结构示意图。下列说法不正确的是 。
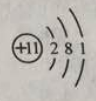
a.钠属于金属元素 b.钠原子的质子数为11
c.钠离子的符号为Na+ d.钠在化学反应中易得到电子
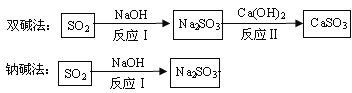
(2)钠与水反应生在氢氧化钠和氢气。化学方程式为 ;小苏打受热分解生成碳酸钠、二氧化碳和水,化学方程式为
(3)配制一瓶下图溶液需氯化钠 g;配置50g6%的氯化钠溶液,若用量筒量取水时俯视读数(其它操作正确),则溶液的质量分数 6%(填“>”“<”或“=”)

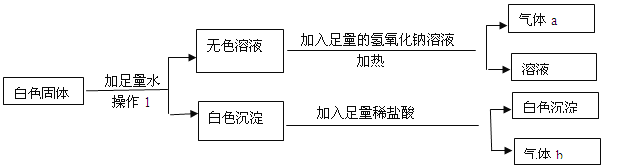
(4)已知:2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2↑。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象?如何检验验证该水溶液中含有的两种溶质。(请简要写出实验步骤及现象)
(5)钛和钛合金性能优良,广泛用于航空、造船和化学工业。工业上常用钠来制取钛,在高温时,钠与四氯化钛反应生成氯化钠和钛。若要用该方法制取2.4kg钛,理论上需要用钠的质量是多少?
【答案】(1)d (2)2Na+2H2O===2NaOH+H2↑ 2NaHCO3Na2CO3+H2O + CO2↑
(3)4.5g,>
(4)产生大量的气泡;加入过量的氯化钙溶液,若产生了沉淀说明含有碳酸根离子,即含有碳酸钠;再向溶液中滴加少量的酚酞,若酚酞试液变红,则证明溶液呈碱性,即含有氢氧化钠
(5)4.8kg
【解析】
试题分析:(1)钠原子的最外层电子数为1,在化学反应中易失去1个电子形成稳定结构,d错误;
(2)根据描述,该反应的反应物是钠和水,生成物是氢氧化钠和氢气表示为2Na+2H2O===2NaOH+H2↑;碳酸氢钠在加热条件下生成碳酸钠、二氧化碳、水,2NaHCO3Na2CO3+H2O + CO2↑
(3)根据标签信息,500ml氯化钠注射液的质量=500ml×1.0g/ml=500g,溶质的质量=500g×0.9%=4.5g;
用量筒量取水时俯视读数,那么读数偏大,即所量的液体的体积偏小,即溶剂的质量偏小,那么溶液的质量也会偏小,故所得溶液的溶质质量分数会偏大;
(4)过氧化钠部分变质,即含有过氧化钠和氢氧化钠或碳酸钠,加入水,过氧化钠与水反应会生成氧气,会产生大量的气泡,氢氧化钠固体溶解放热;要证明氢氧化钠和碳酸钠,实际是验证碳酸根离子和氢氧根离子的存在。可行溶液中加入过量的氯化钙溶液,若产生了沉淀说明含有碳酸根离子,即含有碳酸钠;再向溶液中滴加少量的酚酞,若酚酞试液变红,则证明溶液呈碱性,即含有氢氧化钠;
(5)利用化学方程式,根据反应的质量比即可计算出需要的钠的质量。
设理论上需要用钠的质量为x,
4Na+TiCl4=======4NaCl+Ti
92 48
X 2.4kg
92/48 =x/2.4kg
X=4.8kg
答:略

 优加精卷系列答案
优加精卷系列答案