��Ŀ����
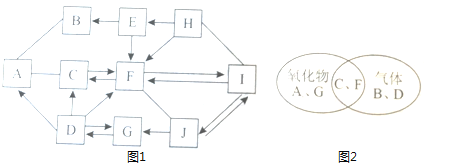
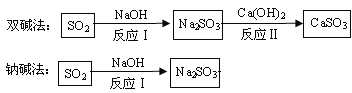
����Ŀ����6������ҵ����ͨ�����ж����������ŷ�ǰ�辭������������ͼ�����ֳ����������к������ʵ�ת��·�������ֲ�����������
��ش��������⣺
��1����Ӧ��Ļ�ѧ����ʽ�� ��
��2����Ӧ�������Ļ�����Ӧ������ ��CaSO3��Ca��S��OԪ�ص��������� ��
��3����֪ԭ��NaOH�ļ۸�Ϊ2.9Ԫ/kg��Ca��OH��2�ļ۸�Ϊ0.36Ԫ/kg�����ֹ����У�������ͬ������SO2��˫������ԭ�ϳɱ����ͣ���ԭ���� ��
���𰸡���1��2NaOH + SO2 ==== Na2SO3 + H2O��
��2�����ֽⷴӦ��5:4:6��
��3����Ӧ���ɵ��������ƿ���ѭ������
��������
�����������1����Ӧ��Ļ�ѧ����ʽ��2NaOH + SO2 ==== Na2SO3 + H2O����2����Ӧ�����ķ�ӦΪ�������ƺ��������ƣ�����������ƺ��������ƣ��κͼ�ķ�Ӧ�������ֽⷴӦ��CaSO3��Ca��S��OԪ�ص���������5:4:6����3����3����֪ԭ��NaOH�ļ۸�Ϊ2.9Ԫ/kg��Ca��OH��2�ļ۸�Ϊ0.36Ԫ/kg�����ֹ����У�������ͬ������SO2��˫������ԭ�ϳɱ����ͣ���ԭ���Ƿ�Ӧ���ɵ���������ѭ�����á�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ