题目内容
【题目】盐城已经迎来高铁时代,高铁的建设过程中使用到大量的铝、铜、铁等金属材料,请按要求填空。
(1)铝合金属于___________(填“纯净物”或“混合物”),铝的抗腐蚀性能较强,是因为______________。(写出化学反应方程式)
(2)为探究铝、铜、铁的金属活动性顺序,某同学选用了下列药品进行实验,其中不能一次性证明的是______(填字母序号)。
A.铜丝、铁丝、氯化铝溶液
B.铝丝、铜丝、硫酸亚铁溶液
C.铝丝、铁丝、铜丝、稀盐酸
D.铁丝、氯化铝溶液、氯化铜溶液
(3)工业炼铁需要铁矿石、石灰石、________和空气等原料。实验小组为探究某铁矿石的主要成分(可表示为FexOy) ,设计如下实验。( 注:铁矿石中杂质不参与反应)
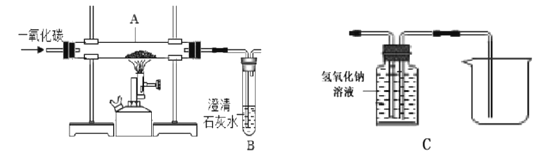
实验步骤:
①取37.3g铁矿石装人硬质玻璃管中
②通人CO 一段时间后加热,A处发生反应的化学方程式是_________________(以氧化铁为例) ;B装置中可观察到的现象是______________________。
③充分反应后测得玻璃管中的固体质量为30.9g,实验反思:某同学认为该装置有明显缺陷,建议在B装置后加C装置,C装置的作用是_____________,_____________。
【答案】混合物 4Al+3O2=2Al2O3 A 焦炭 Fe2O3+3CO![]() 2Fe+3CO2 澄清的石灰水变浑浊 可以收集未参加反应的一氧化碳气体,防止污染空气 吸收二氧化碳
2Fe+3CO2 澄清的石灰水变浑浊 可以收集未参加反应的一氧化碳气体,防止污染空气 吸收二氧化碳
【解析】
(1)铝合金属于含有多种物质成分,属于混合物,铝的抗腐蚀性能较强,是因为:铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,则氧化铝在空气中氧化生成三氧化二铝:4Al+3O2=2Al2O3;
(2)为探究铝、铜、铁的金属活动性顺序,某同学选用了下列药品进行实验,其中不能一次性证明的是:
A、铜丝、铁丝、氯化铝溶液,铜丝和铁丝都不能与氯化铝溶液反应,不能证明铜和铁的金属活动顺序;故选项错误,但符合题意;
B、铝丝、铜丝、硫酸亚铁溶液,铝丝能与硫酸亚铁发生反应,但铜丝不能,说明金属活动顺序:铝>铁>铜;故选项正确,但不符合题意;
C、铝丝、铁丝、铜丝、稀盐酸,铝丝与稀盐酸反应产生气泡速率较快,铁丝与稀盐酸反应产生气泡速率较慢,铜丝不能与稀盐酸反应,说明金属活动顺序:铝>铁>铜;故选项正确,但不符合题意;
D、铁丝、氯化铝溶液、氯化铜溶液,铁丝不能与氯化铝溶液反应,但可以与氯化铜溶液发生置换反应,说明金属活动顺序:铝>铁>铜;故选项正确,但不符合题意;
故选:A。
(3)工业炼铁需要铁矿石、石灰石、焦炭和空气等原料。实验小组为探究某铁矿石的主要成分 ,设计如下实验。
实验步骤:
①取37.3g铁矿石装人硬质玻璃管中
②一氧化碳高温条件下与氧化铁反应产生铁和二氧化碳的化学方程式是:Fe2O3+3CO![]() 2Fe+3CO2;二氧化碳与氢氧化钙反应产生碳酸钙沉淀,B装置中可观察到的现象是:澄清的石灰水变浑浊;
2Fe+3CO2;二氧化碳与氢氧化钙反应产生碳酸钙沉淀,B装置中可观察到的现象是:澄清的石灰水变浑浊;
③充分反应后测得玻璃管中的固体质量为30.9g,实验反思:某同学认为该装置有明显缺陷,建议在B装置后加C装置,C装置的作用是:1、可以收集未参加反应的一氧化碳气体,防止污染空气;2、吸收二氧化碳。

【题目】化学实验过程中产生的废液要经过无害化处理,防止水体污染。在鉴别NaOH溶液和Na2CO3溶液的实验课上,兴趣小组的同学们完成实验后对废液成分展开探究。
通过小组合作,同学们完成了如下图所示的两组小实验。实验中实验_____(填序号)可能出现气泡的现象。生成白色沉淀的反应的化学方程式是_____。
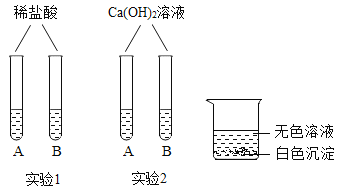
完成试验后,小明将四支试管中的剩余物倒入一个洁净的大烧杯中,充分搅拌、静置,观察到杯内上层是无色溶液,下层有白色沉淀,由此可以确定:上层无色溶液中一定不含的离子是_____(填离子符号)。除了溶液中一定含有氯化钠,小组同学对上层溶液中还可能含有的物质成分进行如下探究。
(提出问题)上层溶液中可能含有什么物质?
(猜想与假设)上层溶液中可能含有NaOH、Na2CO3、Ca(OH)2中的一种或几种。
(进行实验)
实验步骤 | 实现现象 | 实验结论 | |
方案一 | ①取少量溶液于试管中,滴加无色酚酞溶液; ②继续滴加稀盐酸 | ①_____ ②有气泡冒出 | 上层溶液中一定没有_____。 |
方案二 | 取少量溶液于试管中,_____(合理即可,指示剂除外) | _____ | 上层溶液中含有NaOH、Na2CO3。 |
(反思评价)
实验结束后,应将烧杯内物质过滤,滤渣回收,向滤液中加入适量_____(填试剂名称)处理后在排放。