题目内容
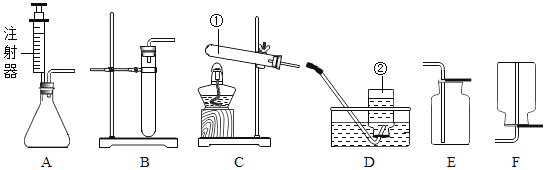
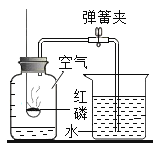
【题目】化学实验是学习化学的基础,请根据下列装置图回答问题。

(1)铁丝在氧气中燃烧的化学方程式为__________________。
(2)铁丝绕成螺旋状的原因是_________。
(3)小明按图示进行实验时,集气瓶炸裂了,其可能的原因是_____________。
(4)图中螺旋状铁丝的末端系一根火柴的作用是__________。
(5)为延长铁丝燃烧的时间,向盛有氧气的集气瓶中插入铁丝的方法是_________________。
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4 mm)放入氧气中燃烧时的实验现象的记录。请你分析后回答问题:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,… |
①你认为表中未填的实验现象是_______。
②造成铁丝在氧气中燃烧时火星四射的主要原因是______。
【答案】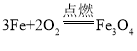 增大与氧气的接触面积 未在瓶中放少量水或铺一层细沙 引燃铁丝 由上而下缓慢插入 火星四射 铁丝中含有的碳引起的
增大与氧气的接触面积 未在瓶中放少量水或铺一层细沙 引燃铁丝 由上而下缓慢插入 火星四射 铁丝中含有的碳引起的
【解析】
(1)铁丝在氧气中燃烧生成四氧化三铁,反应的化学方程式为: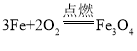 。
。
(2)铁丝绕成螺旋状的原因是增大与氧气的接触面积。
(3)集气瓶中要放少量水或铺一层细沙,防止铁丝燃烧的生成物熔化后溅落炸裂瓶底,说明该反应是放热的。
(4)螺旋状铁丝的末端系一根火柴的作用是引燃铁丝。
(5)为延长铁丝燃烧的时间,向盛有氧气的集气瓶中伸入铁丝的方法是由上而下缓慢插入。
(6)①通过对比可知铁丝含碳越高,火星越多,所以含碳0.6%的铁丝在氧气中燃烧应产生火星四射现象。因此由表中前三个实验的现象可推知,表中未填的实验现象为:火星四射。
②由以上探究可知:铁丝在氧气中燃烧产生火星的多少与含碳量有关,所以铁丝在氧气中燃烧产生火星四射现象的原因是:铁丝中含有的碳引起的。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案