题目内容
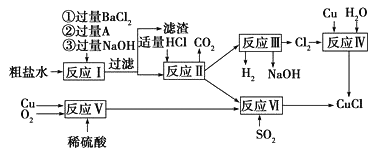
【题目】某化学兴趣小组设计了一个验证某氯化钠溶液中混有碳酸钠、硫酸钠和氢氧化钠的实验方案,实验流程如图所示:
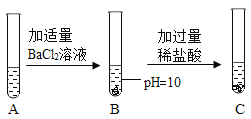
⑴当测得B中溶液的pH=10时,即可判断原溶液中一定混有_____。
⑵向B中加入过量稀盐酸,观察到_____时,完成对剩余物质的验证。
⑶完成实验后,将C中物质过滤,滤液中一定含有的溶质是_____。
【答案】NaOH 有气泡产生,部分白色沉淀消失 NaCl、HCl
【解析】
碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,硫酸钠与氯化钡反应生成硫酸钡沉淀和氯化钠。因此向溶液中加入适量的氯化钡溶液,由于碳酸钠与氯化钡反应生成的碳酸钡沉淀能溶于盐酸,产生气泡,硫酸钠与氯化钡反应生成的沉淀不溶于稀盐酸,测得B中溶液的pH=10时,即可判断原溶液中一定混有氢氧化钠;向B中加入过量稀盐酸,观察到产生气泡,部分白色沉淀消失,且仍有固体剩余时,说明溶液中含有碳酸钠和硫酸钠完成了对剩余物质的验证;因为向B中加入了过量的稀盐酸,所以完成实验后,将C中物质过滤,滤液中一定含有的溶质是氯化氢,同时还有氯化钠。
故答案为:(1)NaOH;(2)有气泡产生,部分白色沉淀消失;(3)NaCl、HCl。

练习册系列答案
相关题目