题目内容
【题目】向一定质量AgNO3和Cu (NO3 )2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( )
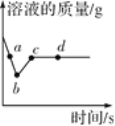
A. 取a点溶液,滴加稀盐酸,无白色沉淀
B. 图标上b~c段质量增加的原因是Zn与Cu(NO3)2溶液反应
C. b点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag
D. c点和d点溶质种类不同,金属单质种类也不同
【答案】B
【解析】A、锌和硝酸银、硝酸铜反应的化学方程式及其质量关系为:
Zn+2AgNO3=Zn(NO3)2+2Ag,Zn+Cu(NO3)2=Zn(NO3)2+Cu,
65216 6564
由以上质量关系可知,锌和硝酸银反应时溶液质量减小,和硝酸铜反应时溶液质量增大,a点时是锌和硝酸银反应的过程,溶液中含有硝酸银,滴加稀盐酸时,稀盐酸和硝酸银反应生成白色沉淀氯化银,正确;B、图标上bc段质量增加的原因是Zn与Cu(NO3)2溶液反应,正确;C、b点时硝酸银恰好完全反应,溶液中金属离子有反应生成的Zn2+和没有反应的Cu2+,金属单质有Zn、Ag,没有Cu,错误;D、c点和d点溶质种类相同,都是硝酸锌,金属单质种类不同,c点时是Ag和Cu,d点时是Zn、Cu、Ag,正确。故选C。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目