题目内容
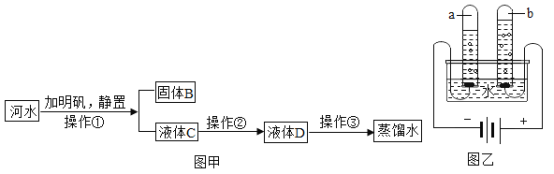
【题目】初中化学实验中,铁钉多次亮相。如图展示了光亮铁钉的一系列变化。
![]()
(1)①中发生反应的化学方程式可以是_____。
(2)②中,铁钉主要与空气中的_____和_____发生反应。
(3)如果用a、b分别代表光亮铁钉和红色铁钉,则它们的质量关系是:a_____b(填“>”、“=”或“<”)。
(4)如图是利用CO还原氧化铁(铁锈的主要成分)的实验装置图,玻璃管中发生反应的化学方程式是_____;处理尾气的方法是_____。

【答案】Fe+CuSO4═Cu+FeSO4 氧气 水 < Fe2O3+3CO![]() 2Fe+3CO2 点燃或用气球收集
2Fe+3CO2 点燃或用气球收集
【解析】
(1)①中铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4;
(2)②中,铁钉主要与空气中的氧气、水共同作用,生成铁锈;
(3)如果用a、b分别代表光亮铁钉和红色铁钉,铁与氧气、水发生化学反应生成铁锈,由质量守恒定律,则它们的质量关系是:a<b;
(4)用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO![]() 2Fe+3CO2;一氧化碳有毒,直接排放到空气中会污染环境,可点燃或用气球收集。
2Fe+3CO2;一氧化碳有毒,直接排放到空气中会污染环境,可点燃或用气球收集。

【题目】铁是世界上年产量最高的金属,铁及其合金也是应用最广泛的金属材料。请根据我们所学的有关金属的知识回答问题:
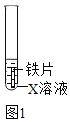
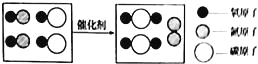
(1)验证金属的活动性(实验装置如图1)
①若要证明Fe在金属活动性顺序中位于氢前,X溶液可选用______,其现象为______。
②若X溶液为少量硫酸铜溶液,该反应的化学方程式为______。待充分反应后,取出铁片,放入金属R,观察到R表面有黑色固体析出。根据上述实验现象,得出Fe、Cu、R的金属活动性顺序为______。
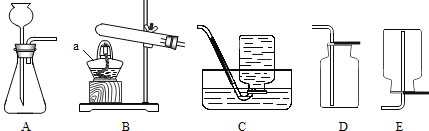
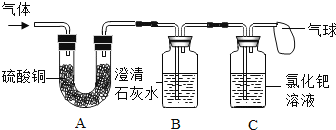
(2)某纯净气体通过如图2装置时,可观察到:A中紫色石蕊试液不变色,C中澄清石灰水变浑浊。请按要求回答问题:
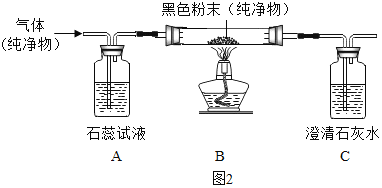
①纯净气体可以是CO.若黑色固体为______,反应过程中B处可以观察到黑色固体______的明显实验现象。
②纯净气体可以是CO.但B处无明显实验现象,则B处发生反应的化学方程式为______。
③纯净气体和黑色固体的组合还可以是______,则B处的实验现象为______。
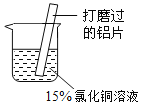
(3)铝是地壳中含量最高的金属元素。某小组同学在实验室研究铝与氯化铜溶液的反应液的反应。
实验操作 | 实验现象 |
| A.红色物质附着于铝片表面 B.铝片表面逸出大量无色气体,放出大量的热 C.烧杯底部出现红色沉淀和白色沉淀 |
①现象A和现象C中的红色物质均为Cu,生成该物质的化学方程式为______。
②经检验,现象B中的无色气体为氢气。甲同学猜测可能是氯化铜溶液显酸性。经实验检测,证实了甲的猜想。
③探究白色沉淀的化学成分。
(推理猜想)
乙同学通过查阅资料认为白色沉淀可能是氯化亚铜(CuCl)。
(查阅资料)
★CuCl可与浓氨水反应生成无色的Cu(NH3)2+和Cl-
★Cu(NH3)2+在空气中易被氧化变为蓝色:Cl-可与硝酸银溶液反应,产生白色沉淀。
(进行实验)
步骤一:取烧杯底部的白色沉淀,充分洗涤;
步骤二:向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
步骤三:取其中一份无色溶液……
步骤四:将另一份无色溶液放置于空气中……
以上步骤三的实验方案是______;
步骤四的现象是______。
(得出结论)通过实验可以确定,该白色固体是CuCl。
(反思与评价)A和CuCl2溶液反应为什么会出现CuCl呢?
丙同学猜测:可能是Cu与CuCl2溶液反应生成了CuCl。
丙同学为了验证猜想,取Cu粉与15%CuCl2溶液混合,无白色沉淀产生。
④丙通过分析Al与CuCl2溶液反应的实验现象,改进了实验,证明了Cu与CuCl2溶液反应生成了CuCl,改进之处是______。
⑤丁同学认为丙同学的实验还不够严谨,还应考虑______对Cu与CuCl2溶液反应的影响。