题目内容
某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。
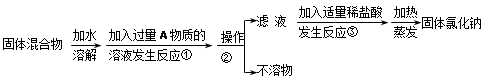
(1)写出A物质的化学式 ,A物质的俗称是 。
(2)操作②的名称是 。
(3)写出反应③的化学方程式 。
(4)反应①中加入过量A物质的目的是 ;反应③中如果加入盐酸也过量,则对所得到的氯化钠纯度是否有影响?理由是 。
(5)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
(填“增大”、“不变”或“减少”)。

(1)写出A物质的化学式 ,A物质的俗称是 。
(2)操作②的名称是 。
(3)写出反应③的化学方程式 。
(4)反应①中加入过量A物质的目的是 ;反应③中如果加入盐酸也过量,则对所得到的氯化钠纯度是否有影响?理由是 。
(5)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
(填“增大”、“不变”或“减少”)。
(1)Na2CO3 , 纯碱
(2)过滤
(3)Na2CO3+2HCl→2NaCl + CO2↑+H2O
(4)使氯化钠中的氯化钙完全反应;(有“除尽”“反应完”等词语,合理给分)
没有,因为盐酸具有挥发性,加热蒸发时过量的盐酸会挥发掉。(合理给分)
(5)增大
(2)过滤
(3)Na2CO3+2HCl→2NaCl + CO2↑+H2O
(4)使氯化钠中的氯化钙完全反应;(有“除尽”“反应完”等词语,合理给分)
没有,因为盐酸具有挥发性,加热蒸发时过量的盐酸会挥发掉。(合理给分)
(5)增大
解(2):从“滤液,不溶物”可以看出操作是过滤。
解(1):从后面看,固体氯化钠是经过加盐酸与滤液反应得到,根据质量守恒定律得知,滤液中一定含有钠元素,而二者要想反应,滤液中必须含有能与氢离子反应的离子,初中常见的与氢离子反应的是碳酸根离子,所以滤液的主要成分是碳酸钠。而滤液有可能是过量的A物质,所以A物质是碳酸钠。俗名纯碱或苏打。
(3)根据化学方程式,Na2CO3+2HCl→2NaCl + CO2↑+H2O
(4)加入过量A是防止氯化钙没有除尽,影响氯化钠的提纯,换言而之,是使氯化钠中的氯化钙完全反应。 根据盐酸的物理性质——易挥发,可知,加热蒸发时过量的盐酸会挥发掉。所以对所得到的氯化钠纯度没有影响 。
(5)因为在反应3中 Na2CO3+2HCl→2NaCl + CO2↑+H2O,生成了NaCl,所以分离后所得氯化钠的质量比分离前原混合物中氯化钠的质量大。
解(1):从后面看,固体氯化钠是经过加盐酸与滤液反应得到,根据质量守恒定律得知,滤液中一定含有钠元素,而二者要想反应,滤液中必须含有能与氢离子反应的离子,初中常见的与氢离子反应的是碳酸根离子,所以滤液的主要成分是碳酸钠。而滤液有可能是过量的A物质,所以A物质是碳酸钠。俗名纯碱或苏打。
(3)根据化学方程式,Na2CO3+2HCl→2NaCl + CO2↑+H2O
(4)加入过量A是防止氯化钙没有除尽,影响氯化钠的提纯,换言而之,是使氯化钠中的氯化钙完全反应。 根据盐酸的物理性质——易挥发,可知,加热蒸发时过量的盐酸会挥发掉。所以对所得到的氯化钠纯度没有影响 。
(5)因为在反应3中 Na2CO3+2HCl→2NaCl + CO2↑+H2O,生成了NaCl,所以分离后所得氯化钠的质量比分离前原混合物中氯化钠的质量大。

练习册系列答案
相关题目