题目内容
【题目】用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的是( )
A. 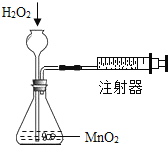 粗略测定氧气的体积
粗略测定氧气的体积
B. 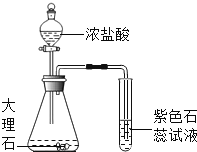 验证CO2与H2O反应生成碳酸
验证CO2与H2O反应生成碳酸
C. 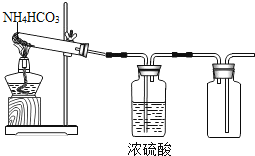 制取并收集干燥的NH3
制取并收集干燥的NH3
D. 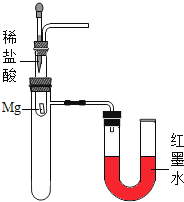 验证Mg和HCl反应的热效应
验证Mg和HCl反应的热效应
【答案】AD
【解析】
A、过氧化氢和二氧化锰混合会生成氧气,产生氧气后锥形瓶内压强变大,会推动注射器活塞向外,所以可用该装置粗略测定O2体积,符合题意;
B、浓盐酸具有挥发性,挥发出的氯化氢气体也能使紫色石蕊试液变红,所以不能用该装置验证CO2与H2O反应生成碳酸,不符合题意;
C、氨气和硫酸反应生成硫酸铵,所以不能用该装置制取并收集干燥的NH3,不符合题意;
D、盐酸和金属镁反应生成氢气氯化镁,同时发出热量,也会使大试管内的气体膨胀,压强增大,会使U形管出现左低右高的现象,所以能验证Mg和HCl反应的热效应,符合题意。故选AD。

 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案【题目】小冬在课外阅读中得知:氢氧化铜受热会分解生成氧化铜和水,于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
(1)请写出加热氢氧化铜的化学方程式为____________________。
(2)小冬在加热氢氧化铜时,发现蓝色固体先变成黑色;继续高温灼烧黑色固体变成红色,同时有气体产生。为弄清这种红色固体的成份,进行了如下的探究:
(查阅资料)Cu和Cu2O均为红色固体,且Cu2O+H2SO4=Cu+CuSO4+H2O。
(提出猜想)红色固体是:Ⅰ.Cu Ⅱ.Cu2O Ⅲ.______________。
(进行实验)
操作 | 现象 | 结论 |
①取灼烧后的红色固体2g于试管中,加入足量稀硫酸,加热并充分振荡,静置。 | _________________ | 红色固体中含有Cu2O |
②过滤、洗涤、干燥。 | 得红色固体 | 红色固体中含有Cu |
(结论分析)据上述现象,小冬认为猜想______成立。你认为小冬的结论是否合理______(填“是”或“否”),理由是_______________________________________。如要证明红色固体的成分,还需要补充的操作是________________________________________。