题目内容
(2010?大庆)为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究(注:该反应还原产物只有铜).
【对固体猜想】
猜想Ⅰ:全部是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、
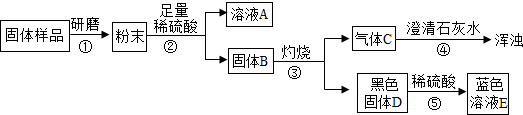
【进行实验】实验流程见下图:
【问题与讨论】
(1)步骤①把固体研成粉末,目的是
(2)C的化学式为
(3)如果溶液A无色,则证明猜想
(4)如果木炭与氧化铜反应充分,则猜想
【对固体猜想】
猜想Ⅰ:全部是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、
木炭
木炭
.【进行实验】实验流程见下图:

【问题与讨论】
(1)步骤①把固体研成粉末,目的是
使物质与稀硫酸充分接触,从而达到分离的目的
使物质与稀硫酸充分接触,从而达到分离的目的
.步骤②包括溶解、过滤
过滤
两步操作,它们共同用到的玻璃仪器是烧杯、玻璃棒
玻璃棒
.(2)C的化学式为
CO2
CO2
,由此推出固体B中含有C、Cu
C、Cu
(写化学式),步骤⑤发生反应的化学方程式为:CuO+H2SO4═CuSO4+H2O
CuO+H2SO4═CuSO4+H2O
.(3)如果溶液A无色,则证明猜想
III
III
成立.(4)如果木炭与氧化铜反应充分,则猜想
Ⅳ
Ⅳ
不成立.分析:【对固体猜想】根据反应物来进行判断;
【问题与讨论】(1)将固体研成粉末可以使物质与稀硫酸充分接触,从而达到分离的目的,根据过滤和溶解的操作来选择合适的仪器;
(2)二氧化碳能使澄清石灰水变浑浊的气体,而溶液显蓝色的是硫酸铜溶液.根据④⑤的现象推导出固体B的组成;
(3)加硫酸反应后溶液呈无色,溶液中无硫酸铜,进而可以判断固体粉末的成分;
(4)根据木炭和氧化铜反应的产物来分析并作出判断.
【问题与讨论】(1)将固体研成粉末可以使物质与稀硫酸充分接触,从而达到分离的目的,根据过滤和溶解的操作来选择合适的仪器;
(2)二氧化碳能使澄清石灰水变浑浊的气体,而溶液显蓝色的是硫酸铜溶液.根据④⑤的现象推导出固体B的组成;
(3)加硫酸反应后溶液呈无色,溶液中无硫酸铜,进而可以判断固体粉末的成分;
(4)根据木炭和氧化铜反应的产物来分析并作出判断.
解答:解:【对固体猜想】根据反应可以知道,如果反应不充分则会含有木炭,故猜想Ⅳ中应该含有木炭;
【问题与讨论】(1)将固体研成粉末可以使物质与稀硫酸充分接触,从而达到分离的目的;而分离固体和液体常用过滤的方法,在过滤和溶解的过程中都要用到玻璃棒;
(2)二氧化碳可以使澄清石灰水变浑浊,而反应⑤中溶液为蓝色溶液,该蓝色溶液为硫酸铜溶液,所以黑色固体D为氧化铜,而第②步中所加入的硫酸是足量的,所以说明在固体B中含有的物质为木炭和铜,而铜灼烧之后产生的氧化铜和硫酸反应生成了硫酸铜溶液;
(3)如果溶液A为无色溶液,则溶液中没有硫酸铜,所以可以推断在混合物中不含氧化铜,结合(2)的解答可以知道猜想III是正确的;
(4)如果木炭和氧化铜充分反应,则产物为铜和二氧化碳,所以猜想Ⅳ不正确.
故答案为:
【对固体猜想】木炭;
【问题与讨论】
(1)使物质与稀硫酸充分接触,从而达到分离的目的;过滤;玻璃棒;
(2)CO2;C、Cu;CuO+H2SO4═CuSO4+H2O;
(3)III;
(4)Ⅳ.
【问题与讨论】(1)将固体研成粉末可以使物质与稀硫酸充分接触,从而达到分离的目的;而分离固体和液体常用过滤的方法,在过滤和溶解的过程中都要用到玻璃棒;
(2)二氧化碳可以使澄清石灰水变浑浊,而反应⑤中溶液为蓝色溶液,该蓝色溶液为硫酸铜溶液,所以黑色固体D为氧化铜,而第②步中所加入的硫酸是足量的,所以说明在固体B中含有的物质为木炭和铜,而铜灼烧之后产生的氧化铜和硫酸反应生成了硫酸铜溶液;
(3)如果溶液A为无色溶液,则溶液中没有硫酸铜,所以可以推断在混合物中不含氧化铜,结合(2)的解答可以知道猜想III是正确的;
(4)如果木炭和氧化铜充分反应,则产物为铜和二氧化碳,所以猜想Ⅳ不正确.
故答案为:
【对固体猜想】木炭;
【问题与讨论】
(1)使物质与稀硫酸充分接触,从而达到分离的目的;过滤;玻璃棒;
(2)CO2;C、Cu;CuO+H2SO4═CuSO4+H2O;
(3)III;
(4)Ⅳ.
点评:本考点属于科学探究题,既有对实验方案的设计和评价,又有碳的还原性、化学方程式的书写;有关的实验设计也是中考的重要考查内容之一,特别是对实验方案的评价是一个重点也是一个难点,同学们应该认真掌握,综合应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目