题目内容
【题目】广州市食品药品监督管理局2013年5月16日公布餐饮环节一季度食品抽检数据,在抽检的18批次米及米制品产品中,有8批次产品镉超标。镉是一种重金属,会抑制人体钙质吸收。体内镉超标易患骨质疏松、骨痛病等病症。镉是银白色有光泽的金属,高温下也可与硫直接化合,生成硫化镉。氧化镉和氢氧化镉的溶解度都很小,它们溶于酸,但不溶于碱。认真阅读以上材料回答以下问题:
(1)如图是镉(Cd)原子的构成示意图,根据图示信息回答下列问题:
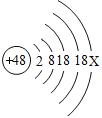
①图中X的值为_____,在化学反应中镉原子容易_____(“得到”或“失去”)电子:形成离子符号表示为_____。
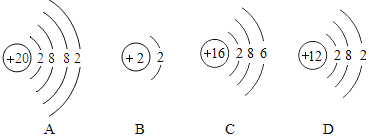
②镉原子与下列元素化学性质相似的是_____。
(2)写出镉与硫直接化合反应的化学方程式:_____。
(3)某企业想将含氢氧化镉的镉渣用硫酸处理掉,请你写出反应的化学方程式:_____。
【答案】2 失去 Cd2+ A、D Cd+S![]() CdS Cd(OH)2+H2SO4=CdSO4+2H2O
CdS Cd(OH)2+H2SO4=CdSO4+2H2O
【解析】
(1)①在原子中质子数=核外电子数;故x=48-2-8-18-18=2;镉(Cd)原子最外层电子数为2,易失去最外层的电子形成带两个单位正电荷的镉离子;
②最外层电子数相同的元素化学性质相似,B只有一个电子层,最外层是两个电子的稳定结构,镉原子与AD最外层电子数相同故化学性质相似;
(2)镉在高温下也可与硫直接化合,生成硫化镉,反应的化学方程式:Cd+S![]() CdS;
CdS;
(3)氢氧化镉与硫酸反应生成硫酸镉和水,反应的化学方程式为:Cd(OH)2+H2SO4═CdSO4+2H2O;
答案:(1)①2;失去电子;②A、D;
(2)Cd+S![]() CdS;
CdS;
(3)溶于,Cd(OH)2+H2SO4═CdSO4+2H2O.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目