题目内容
某化学兴趣小组对一包干燥的红色粉末组成进行探究。请你参与并回答问题。
【教师提醒】它由Cu 、Fe2O3两种固体中的一种或两种组成。
【提出猜想】红色粉末可能的组成,
猜想①:只有Cu;猜想②:只有 ;猜想③:是Cu 、Fe2O3的混合物
【实验探究】
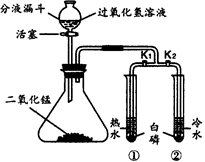
同学们为确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右下图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,继续通CO气体直至玻璃管冷却。

(1)在装置A中先通CO气体的目的是 。A装置中发生反应的化学方程式 ;实验中观察到A装置中的现象为 。
(2)反应前后称量相关装置和物质的总质量,其数据如下表:
小蒋同学初步分析表中的数据后,马上得出猜想 (填“①”“②”“③”)肯定不正确,理由是 。
(3)小林同学认为为了防止溶液倒吸,本实验停止加热前应 先断开A和B的连接,你认为是否需要? (填“需要”或“不需要”),理由是 。
【反思评价】实验后小组内有同学指出:上图装置未进行尾气的处理。于是有同学设计了用右图装置代替原装置,则C装置的作用有 、 (至少答两点)。
【教师提醒】它由Cu 、Fe2O3两种固体中的一种或两种组成。
【提出猜想】红色粉末可能的组成,
猜想①:只有Cu;猜想②:只有 ;猜想③:是Cu 、Fe2O3的混合物
【实验探究】
同学们为确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右下图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,继续通CO气体直至玻璃管冷却。

(1)在装置A中先通CO气体的目的是 。A装置中发生反应的化学方程式 ;实验中观察到A装置中的现象为 。
(2)反应前后称量相关装置和物质的总质量,其数据如下表:
| 反应前 | 反应后 |
| 玻璃管和红色粉末的总质量为37.3 g | 玻璃管和固体物质的总质量为36.1 g |
小蒋同学初步分析表中的数据后,马上得出猜想 (填“①”“②”“③”)肯定不正确,理由是 。
(3)小林同学认为为了防止溶液倒吸,本实验停止加热前应 先断开A和B的连接,你认为是否需要? (填“需要”或“不需要”),理由是 。
【反思评价】实验后小组内有同学指出:上图装置未进行尾气的处理。于是有同学设计了用右图装置代替原装置,则C装置的作用有 、 (至少答两点)。

【提出猜想】Fe2O3(名称、化学式均可)
【实验探究】(1)排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸);3CO + Fe2O3 2Fe + 3CO2 ;红色粉末变黑 (2) ① ; 因为如果固体中只有铜,则固体质量不会减少 (3)不需要;因为一直通入CO气体,B中溶液不会倒吸到A装置中。【反思评价】收集一氧化碳、吸收二氧化碳、检验二氧化碳、防止一氧化碳污染空气。(合理即可)
2Fe + 3CO2 ;红色粉末变黑 (2) ① ; 因为如果固体中只有铜,则固体质量不会减少 (3)不需要;因为一直通入CO气体,B中溶液不会倒吸到A装置中。【反思评价】收集一氧化碳、吸收二氧化碳、检验二氧化碳、防止一氧化碳污染空气。(合理即可)
【实验探究】(1)排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸);3CO + Fe2O3
 2Fe + 3CO2 ;红色粉末变黑 (2) ① ; 因为如果固体中只有铜,则固体质量不会减少 (3)不需要;因为一直通入CO气体,B中溶液不会倒吸到A装置中。【反思评价】收集一氧化碳、吸收二氧化碳、检验二氧化碳、防止一氧化碳污染空气。(合理即可)
2Fe + 3CO2 ;红色粉末变黑 (2) ① ; 因为如果固体中只有铜,则固体质量不会减少 (3)不需要;因为一直通入CO气体,B中溶液不会倒吸到A装置中。【反思评价】收集一氧化碳、吸收二氧化碳、检验二氧化碳、防止一氧化碳污染空气。(合理即可)试题分析:【提出猜想】根据物质的特征颜色,可以推求出猜想②:只有氧化铁;
【实验探究】因为一氧化碳具有可燃性为防止发生爆炸,故(1)在装置A中先通CO气体的目的是排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸),A装置中发生反应的化学方程式:3CO + Fe2O3
 2Fe + 3CO2实验中观察到A装置中的现象为红色粉末变黑;(2)小蒋同学初步分析表中的数据后,马上得出猜想①,肯定不正确,理由是因为如果固体中只有铜,则固体质量不会减少,(3)小林同学认为为了防止溶液倒吸,本实验停止加热前应先断开A和B的连接,是不需要的操作,因为未了防止生成的铁被氧化,一氧化碳一直通入,B中溶液不会倒吸到A装置中。
2Fe + 3CO2实验中观察到A装置中的现象为红色粉末变黑;(2)小蒋同学初步分析表中的数据后,马上得出猜想①,肯定不正确,理由是因为如果固体中只有铜,则固体质量不会减少,(3)小林同学认为为了防止溶液倒吸,本实验停止加热前应先断开A和B的连接,是不需要的操作,因为未了防止生成的铁被氧化,一氧化碳一直通入,B中溶液不会倒吸到A装置中。【反思评价】实验后小组内有同学指出:上图装置未进行尾气的处理。于是有同学设计了用右图装置代替原装置,则C装置的作用有收集一氧化碳、吸收二氧化碳等

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目