题目内容
【题目】欲测定Cu﹣Zn合金及Cu﹣Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器.
(1)你认为能测出的质量分数的是________________合金.
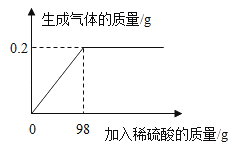
(2)取该合金的粉末26g加入该稀硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示.请计算该合金中铜的质量分数?________________
【答案】Cu—Zn 合金解:设合金中锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
![]() =
= ![]()
x=6.5g
合金中铜的质量为:26g﹣6.5g=19.5g
合金中铜的质量分数=19.5g/26g×100%=75%
答:合金中铜的质量分数为75%.
【解析】
(1)Cu﹣Zn;(2)可根据锌与硫酸反应的化学方程式,利用锌和氢气在反应中的质量关系求解出合金中含锌的质量。进一步求出铜的质量及其中合金中的质量分数
解:(1)在铜银合金中,两种金属的活动性均在氢的后面。所以都不能和酸发生反应。因此无法测出其中的成分。在铜锌合金中,铜不与酸反应,锌能与酸反应生成氢气。所以可通过测量生成氢气的质量(或固体与酸充分反应后的减少的质量),得知金属锌的质量。进一步求出铜的质量分数。即现有条件下能测出铜锌合金中铜的质量分数。
(2)解:设合金中锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
![]() =
= ![]()
x=6.5g
合金中铜的质量为:26g﹣6.5g=19.5g
合金中铜的质量分数= ![]() ×100%=75%
×100%=75%
答:合金中铜的质量分数为75%.

练习册系列答案
相关题目