题目内容
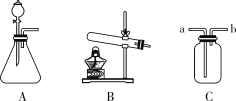
【题目】(2018枣庄改编)请分析下列实验装置,阅读所给材料,回答问题。
材料:氨气(NH3)常温下是一种具有刺激性气味的无色气体,对人体有较大毒性,密度比空气小,极易溶于水,其水溶液显碱性。实验室可用加热氯化铵(NH4Cl)和熟石灰两种固体的方法制取氨气,同时生成氯化钙和水。铵盐易溶于水,Ca(OH)2微溶于水,CaCl2溶液显中性,NH4Cl溶液显酸性。
(1)实验室制取氨气的化学方程式为________,应选取的发生装置是________(填装置编号)。
(2)用C装置收集氨气时,证明气体已经收集满的方法是_________。
(3)某同学对充分反应后反应器内的固体物质做进一步研究:
(提出问题)固体物质的成分是什么?
(作出猜想)猜想Ⅰ:Ca(OH)2、NH4Cl和CaCl2
猜想Ⅱ:Ca(OH)2和CaCl2
猜想Ⅲ:NH4Cl和CaCl2
猜想Ⅳ:只有CaCl2
有同学对上述猜想提出质疑:有一种猜想不合理。你认为是______________。
(实验探究)①取反应器内少量固体于试管中,加水溶解、过滤,得到滤液。
②取少量滤液于试管中,滴加无色酚酞溶液,溶液颜色无变化,说明_____(填一种猜想)不正确。
③再取少量滤液于另一试管中,滴加AgNO3溶液,产生白色沉淀,该同学认为固体中含有NH4Cl,于是得出结论:猜想Ⅲ正确。你认为该同学的结论是否合理并说明理由__________。
(评价反思)该同学认为实验装置仍有不足之处,请你提出改进措施:___________。
【答案】2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O B 将湿润的红色石蕊试纸放在集气瓶a端,红色石蕊试纸变蓝 猜想Ⅰ 猜想Ⅱ 不合理,任一猜想的固体中均含有CaCl2,CaCl2和AgNO3溶液反应也会产生白色沉淀(合理即可) 增加尾气处理装置
CaCl2+2NH3↑+2H2O B 将湿润的红色石蕊试纸放在集气瓶a端,红色石蕊试纸变蓝 猜想Ⅰ 猜想Ⅱ 不合理,任一猜想的固体中均含有CaCl2,CaCl2和AgNO3溶液反应也会产生白色沉淀(合理即可) 增加尾气处理装置
【解析】
(1)实验室可用加热氯化铵和熟石灰两种固体的方法制取氨气,反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;反应物为固体,反应条件需要加热,故应选取的发生装置是固固加热型装置B。(2)氨气的密度比空气小,用C装置收集时应b进a出,故检验氨气收集满时,应将湿润的红色石蕊试纸放在集气瓶a导管端,若红色石蕊试纸变蓝色,则氨气收集满。(3)【作出猜想】根据题给信息,Ca(OH)2和NH4Cl充分发生反应,不可能同时共存,故猜想Ⅰ不合理。【实验探究】②滴加无色酚酞溶液,溶液颜色无变化,说明溶液不显碱性,故固体中不含Ca(OH)2,猜想Ⅱ不正确;③取少量滤液于另一试管中,滴加AgNO3溶液,产生白色沉淀,只能说明原滤液中含有氯离子,但不能得出猜想Ⅲ正确的结论,所以该同学的结论不合理。【评价反思】氨气是有刺激性气味的有毒气体,故应增加尾气处理装置来吸收氨气。
CaCl2+2NH3↑+2H2O;反应物为固体,反应条件需要加热,故应选取的发生装置是固固加热型装置B。(2)氨气的密度比空气小,用C装置收集时应b进a出,故检验氨气收集满时,应将湿润的红色石蕊试纸放在集气瓶a导管端,若红色石蕊试纸变蓝色,则氨气收集满。(3)【作出猜想】根据题给信息,Ca(OH)2和NH4Cl充分发生反应,不可能同时共存,故猜想Ⅰ不合理。【实验探究】②滴加无色酚酞溶液,溶液颜色无变化,说明溶液不显碱性,故固体中不含Ca(OH)2,猜想Ⅱ不正确;③取少量滤液于另一试管中,滴加AgNO3溶液,产生白色沉淀,只能说明原滤液中含有氯离子,但不能得出猜想Ⅲ正确的结论,所以该同学的结论不合理。【评价反思】氨气是有刺激性气味的有毒气体,故应增加尾气处理装置来吸收氨气。

【题目】(2017石家庄质检二模)某研究性学习小组欲测定生铁中的含碳量,采用的方法如下:取生铁样品5.8 g,把50 g稀硫酸分5次加入到生铁样品中,实验过程中的数据见下表(假设生铁样品中只含铁和碳)。请计算:
加入硫酸的次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
稀硫酸质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体质量/g | 4.4 | 3.0 | 1.6 | 0.2 | 0.2 |
(1)5.8 g生铁中含碳的质量为________g。
(2)所用稀硫酸中溶质的质量分数。
【题目】(2018深圳改编)某Ca(OH)2样品已变质,且只有CaCO3一种杂质,取10 g该样品,将样品放入到足量的盐酸中,所得数据如下表:
时间/s | t0 | t1 | t2 | t3 |
烧杯中剩余物质的质量/g | 280 | 278.9 | 277.8 | 277.8 |
求:(1)生成二氧化碳的质量为_____g。
(2)该样品中Ca(OH)2的质量分数。
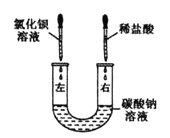
【题目】某化学活动小组在一次实验中进行如下图所示实验:
此时双察到U型管左右两侧产生的現象分別是__________:实验后,小組同学充分振荡U型管,发现管内仍有白色固体残留,将混合物过滤后,同学们对滤液成分产生了浓厚的兴趣,于是进行了进一歩的探究活动。
[提出向題]:滤液中可能含有哪些溶质?
[猜想与假设]:猜想一:溶质为NaC1
猜想二:溶质为NaC1和![]()
猜想三:溶质为NaC1、![]() 和 HCl
和 HCl
[评价与交流]:你认为以上猜想_________不合理,理由是_______________:
则你的猜想为_______________:
[实验探究]:小红为了验证滤液成分,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此得出结论:猜想一成立。小刚认为小红的结论不严密,因为_____。
为验证你的猜想请填写下表:
实验过程 | 实验现象 | 实验结论 |
________ | ________ | 你的猜想成立 |
(归纳与总结]:通过上述实验我们能够总结出:在确定化学反应后所得溶液中溶质成分时,除了考虑生成物外,还要考虑________。
【题目】(2018邯郸一模)为了测定某氢氧化钠溶液的浓度,取20.0 g该溶液于烧杯中,逐滴加入溶质质量分数为7.3 %的稀盐酸,用pH计测定溶液的pH,所得数据如下表:
加入稀盐酸的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
(1)当滴加稀盐酸的质量为9.8 g时,溶液中的溶质是____________。
(2)计算所测氢氧化钠溶液中溶质的质量分数。